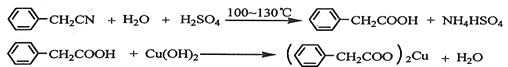
2.对于反应X(g)+Y(g)?3Z(g)(正反应为吸热反应),下列可作为平衡状态的标志的是( )
①单位时间内,A、B生成C的分子数与分解C的分子数相等
②体系的温度不再变化
③外界条件不变时,A、B的浓度不随时间而变化
④体系的压强不再变化
⑤体系的分子总数不再变化.
①单位时间内,A、B生成C的分子数与分解C的分子数相等
②体系的温度不再变化
③外界条件不变时,A、B的浓度不随时间而变化
④体系的压强不再变化
⑤体系的分子总数不再变化.
| A. | ①③⑤ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④⑤ |
19.一定温度下,2L密闭容器中充入0.40mol N2O4,发生反应:N2O4(g)?2NO2(g),一段时间后达到平衡,测得数据如下:
请回答:
(1)20s内,v(NO2)=0.006mol•L-1•s-1.
(2)升高温度时,气体颜色加深,则正反应是吸热(填“放热”或“吸热”)反应.
(3)该温度下反应的化学平衡常数数值为1.8.
(4)相同温度下,若开始时向该容器中充入的是0.20molN2O4和0.40molNO2,则达到平衡后,c(NO2)=0.30mol/L.
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
(1)20s内,v(NO2)=0.006mol•L-1•s-1.
(2)升高温度时,气体颜色加深,则正反应是吸热(填“放热”或“吸热”)反应.
(3)该温度下反应的化学平衡常数数值为1.8.
(4)相同温度下,若开始时向该容器中充入的是0.20molN2O4和0.40molNO2,则达到平衡后,c(NO2)=0.30mol/L.
17.下列化学性质中,苯不具备的是( )
| A. | 可以在空气中燃烧 | B. | 与Br2发生取代反应 | ||
| C. | 与H2发生加成反应 | D. | 能使高锰酸钾溶液褪色 |
16.下列说法不正确的是( )
| A. | 碳酸铵在室温下能自发发生分解,是由于反应生成了易挥发的气体,使体系的熵增大 | |
| B. | 同一种物质气态时熵值最大,液态时次之,而固态时熵值最小 | |
| C. | 与外界隔离的体系,自发过程将导致体系的熵减小 | |
| D. | 在一定条件下,非自发进行的反应也能够发生 |
14.在某一容积为2L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O (g)?CO2(g)+H2(g)△H=a kJ/mol.反应达到平衡后,测得c(CO):c(CO2)=3:2.下列说法正确的是( )
0 159603 159611 159617 159621 159627 159629 159633 159639 159641 159647 159653 159657 159659 159663 159669 159671 159677 159681 159683 159687 159689 159693 159695 159697 159698 159699 159701 159702 159703 159705 159707 159711 159713 159717 159719 159723 159729 159731 159737 159741 159743 159747 159753 159759 159761 159767 159771 159773 159779 159783 159789 159797 203614
| A. | 判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等 | |
| B. | 反应放出的热量为0.04 a kJ | |
| C. | 平衡时H2O的转化率为40% | |
| D. | 若将容器的体积压缩为1 L,有利于该反应平衡正向移动 |
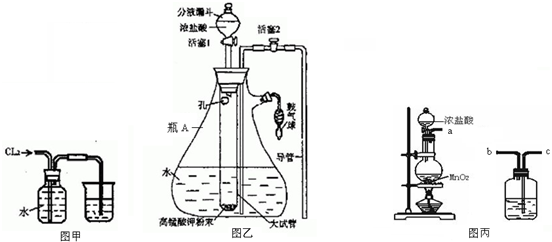
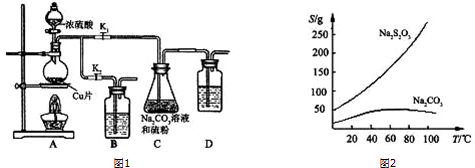
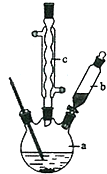 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: