13.某同学用工业硫酸铜(含硫酸亚铁等杂质)制备纯净的CuSO4•5H2O.工艺流程如下(部分操作和条件略):
I.取工业硫酸铜固体,用稀硫酸溶解,过滤.
II.向滤液中滴加H2O2溶液,稍加热.
III.向II的溶液中加入CuO粉末至pH=4.
IV.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1.
V.蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得晶体.
已知部分阳离子生成氢氧化物的pH、Ksp(25℃)如下表:
(1)II中发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)II中将Fe2+氧化为Fe3+的目的是在调节在pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀.
(3)用K3[Fe(CN)6](铁氰化钾)验证II中Fe2+是否转化完全的现象是若有蓝色沉淀生说,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化.
(4)III中发生反应的离子方程式是2Fe3++3CuO+3H2O=2Fe(OH)3+3Cu2+.
通过计算说明在此条件下的溶液中Fe3+是否沉淀完全(提示:当溶液中某离子浓度小于1.0×10-5 mol•L-1时可认为该离子沉淀完全).
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因用稀硫酸酸化至PH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体
(6)V中获得晶体的方法是蒸发浓缩、冷却结晶.
I.取工业硫酸铜固体,用稀硫酸溶解,过滤.
II.向滤液中滴加H2O2溶液,稍加热.
III.向II的溶液中加入CuO粉末至pH=4.
IV.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1.
V.蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得晶体.
已知部分阳离子生成氢氧化物的pH、Ksp(25℃)如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀时pH | 2.7 | 7.6 | 4.7 |
| 完全沉淀时pH | 3.7 | 9.6 | 6.7 |
| Ksp | 4.0×10-38 | 8.0×10-16 | 2.2×10-20 |
(2)II中将Fe2+氧化为Fe3+的目的是在调节在pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀.
(3)用K3[Fe(CN)6](铁氰化钾)验证II中Fe2+是否转化完全的现象是若有蓝色沉淀生说,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化.
(4)III中发生反应的离子方程式是2Fe3++3CuO+3H2O=2Fe(OH)3+3Cu2+.
通过计算说明在此条件下的溶液中Fe3+是否沉淀完全(提示:当溶液中某离子浓度小于1.0×10-5 mol•L-1时可认为该离子沉淀完全).
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因用稀硫酸酸化至PH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体
(6)V中获得晶体的方法是蒸发浓缩、冷却结晶.
10.CO是高炉炼铁的主要反应物之一,发生的主要反应为$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
该反应的平衡常数表达式K=$\frac{c(C{O}_{2})}{c(CO)}$,△H<0(填“>”、“<”或“=”).
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1 000 | 1 150 | 1 300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
9.环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如下:
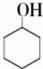 $→_{Na_{2}Cr_{2}O_{7}+H_{2}SO_{4}}^{55℃~69℃}$
$→_{Na_{2}Cr_{2}O_{7}+H_{2}SO_{4}}^{55℃~69℃}$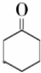
环己醇和环己酮的部分物理性质见下表:
现以20mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯.
分离提纯过程中涉及到的主要步骤有(未排序):
a.蒸馏,除去乙醚后,收集151℃~156℃馏分;
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;
c.过滤;
d.往液体中加入NaCl固体至饱和,静置,分液;
e.加入无水MgSO4固体,除去有机物中少量水.
回答下列问题:
(1)上述分离提纯步骤的正确顺序是d b e c a(填字母).
(2)b中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量.
(3)以下关于萃取分液操作的叙述中,正确的是③.
①振荡几次后需打开分液漏斗上口的玻璃塞放气
②经几次振荡并放气后,手持分液漏斗静置待液体分层
③分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是降低环己酮的溶解度,增加水层的密度,有利于分层.蒸馏除乙醚的操作中采用的加热方式为水浴加热.
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水.
(6)恢复至室温时,分离得到纯产品体积为 12mL,则环己酮的产率约是60%.
 $→_{Na_{2}Cr_{2}O_{7}+H_{2}SO_{4}}^{55℃~69℃}$
$→_{Na_{2}Cr_{2}O_{7}+H_{2}SO_{4}}^{55℃~69℃}$
环己醇和环己酮的部分物理性质见下表:
| 物质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
| 环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
分离提纯过程中涉及到的主要步骤有(未排序):
a.蒸馏,除去乙醚后,收集151℃~156℃馏分;
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层;
c.过滤;
d.往液体中加入NaCl固体至饱和,静置,分液;
e.加入无水MgSO4固体,除去有机物中少量水.
回答下列问题:
(1)上述分离提纯步骤的正确顺序是d b e c a(填字母).
(2)b中水层用乙醚萃取的目的是使水层中少量的有机物进一步被提取,提高产品的产量.
(3)以下关于萃取分液操作的叙述中,正确的是③.
①振荡几次后需打开分液漏斗上口的玻璃塞放气
②经几次振荡并放气后,手持分液漏斗静置待液体分层
③分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是降低环己酮的溶解度,增加水层的密度,有利于分层.蒸馏除乙醚的操作中采用的加热方式为水浴加热.
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是停止加热,冷却后通自来水.
(6)恢复至室温时,分离得到纯产品体积为 12mL,则环己酮的产率约是60%.
7.在密闭容器中给CO和水蒸气的混合物加到800℃时,有下列平衡:CO+H2O?CO2+H2且K=1,若用2molCO和10molH2O(气)相互混合并加热到800℃,达平衡时CO的转化率约为( )
| A. | 16.7% | B. | 50% | C. | 66.7% | D. | 83% |
5.高炉炼铁的烟尘中主要含有锌、铁、铜等金属元素.从烟尘中提取硫酸锌,可以变废为宝,减少其对环境的危害.下图是用高炉烟尘制取硫酸锌的工业流程.

已知:
①20℃时,0.1mol.L-1的金属离子沉淀时的pH
②过二硫酸铵是一种强氧化剂.
③ZnSO4+4NH3=[Zn(NH3)4]SO4,[Zn(NH3)4]SO4易溶于水.
回答下列问题:
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?
(举出1种)增大硫酸浓度或升高温度或边加硫酸边搅拦或增加浸出时间等.
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是pH计(或者酸度计或试纸).
(3)加入MnO2的目的是将Fe2+氧化成Fe3+.
(4)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式MnSO4+(NH4)2S2O8+2H2O=MnO2+(NH4)2SO4+2H2SO4.
(5)写出还原过程发生的主要反应的离子方程式Zn+Cu2+=Zn2++Cu.
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是C.
A锌粉 B氨水 C( NH4)2CO3 D NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值.

已知:
①20℃时,0.1mol.L-1的金属离子沉淀时的pH
| pH | Fe3+ | Zn2+ | Mn2+ | Cu2+ |
| 开始沉淀 | 1.9 | 6.0 | 8.1 | 4.7 |
| 沉淀完全 | 3.7 | 8.0 | 10.1 | 6.7 |
| 沉淀溶解 | 不溶解 | 10.5 | 不溶解 | / |
③ZnSO4+4NH3=[Zn(NH3)4]SO4,[Zn(NH3)4]SO4易溶于水.
回答下列问题:
(1)为提高烟尘中金属离子的浸出率,除了适度增加硫酸浓度外,还可以采取什么措施?
(举出1种)增大硫酸浓度或升高温度或边加硫酸边搅拦或增加浸出时间等.
(2)上述流程测得溶液pH=5.0,此处可以选择的测量仪器是pH计(或者酸度计或试纸).
(3)加入MnO2的目的是将Fe2+氧化成Fe3+.
(4)写出过二硫酸铵把硫酸锰(MnSO4)氧化的化学方程式MnSO4+(NH4)2S2O8+2H2O=MnO2+(NH4)2SO4+2H2SO4.
(5)写出还原过程发生的主要反应的离子方程式Zn+Cu2+=Zn2++Cu.
(6)操作甲中为使锌离子完全沉淀,添加的最佳试剂是C.
A锌粉 B氨水 C( NH4)2CO3 D NaOH
(7)若pH=5.0时,溶液中的Cu2+尚未开始沉淀,求溶液中允许的Cu2+浓度的最大值.
4.某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH+HCl
(三氯乙酸)
②相关物质的相对分子质量及部分物理性质:
(1)仪器A中发生反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;装置B中的试剂是饱和食盐水.
(2)若撤去装置C,可能导致装置D中副产物CCl3COOH、C2H5Cl(填化学式)的量增加;装置D可采用水浴加热的方法以控制反应温度在70℃左右.
(3)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行,为什么?不可行,CCl3COOH溶于乙醇与CCl3CHO.
(4)装置E中可能发生的无机反应的离子方程式有Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(5)测定产品纯度:称取产品0.30g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mo1•L-1Na2S2O3溶液滴定至终点.进行平行实验后,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为88.5%.(CCl3CHO的相对分子质量为147.5)
滴定的反应原理,:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑ I2+2S2O32-═2I-+S4O62-
(6)已知:常温下Ka(CCl3COOH)=1.0×10-1mol•L-1,Ka (CH3COOH)=1.7×10-5mol•L-1
请设计实验证明三氯乙酸、乙酸的酸性强弱.
0 159598 159606 159612 159616 159622 159624 159628 159634 159636 159642 159648 159652 159654 159658 159664 159666 159672 159676 159678 159682 159684 159688 159690 159692 159693 159694 159696 159697 159698 159700 159702 159706 159708 159712 159714 159718 159724 159726 159732 159736 159738 159742 159748 159754 159756 159762 159766 159768 159774 159778 159784 159792 203614

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH+HCl
(三氯乙酸)
②相关物质的相对分子质量及部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水,可溶于乙醇 |
(2)若撤去装置C,可能导致装置D中副产物CCl3COOH、C2H5Cl(填化学式)的量增加;装置D可采用水浴加热的方法以控制反应温度在70℃左右.
(3)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行,为什么?不可行,CCl3COOH溶于乙醇与CCl3CHO.
(4)装置E中可能发生的无机反应的离子方程式有Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(5)测定产品纯度:称取产品0.30g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mo1•L-1Na2S2O3溶液滴定至终点.进行平行实验后,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为88.5%.(CCl3CHO的相对分子质量为147.5)
滴定的反应原理,:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑ I2+2S2O32-═2I-+S4O62-
(6)已知:常温下Ka(CCl3COOH)=1.0×10-1mol•L-1,Ka (CH3COOH)=1.7×10-5mol•L-1
请设计实验证明三氯乙酸、乙酸的酸性强弱.
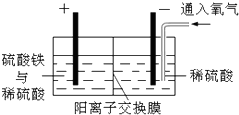 以黄铜矿精矿为原料,制取金属铜的工艺如下所示:
以黄铜矿精矿为原料,制取金属铜的工艺如下所示: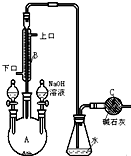 制备溴苯的实验装置如右图所示,请回答下列问题:
制备溴苯的实验装置如右图所示,请回答下列问题: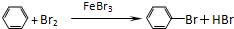 .
. +Br+→[
+Br+→[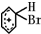 ];[
];[ ]+FeBr4-→
]+FeBr4-→ +HBr+FeBr3.由上述反应可推知:
+HBr+FeBr3.由上述反应可推知: +Br2→
+Br2→ +HBr 中的催化剂为BD.(填字母)
+HBr 中的催化剂为BD.(填字母)