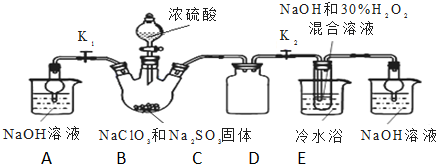
7.碘化钠在医药中用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,也用作食品添加剂、感光剂等. 工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下:
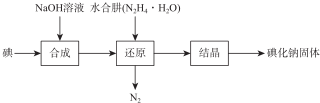
已知:N2H4•H2O在100℃以上分解.
(1)已知,在合成过程的反应产物中含有NalO3,则在合成过程中消耗了3mol I2,所生成 NalO3的物质的量为1mol.
(2)写出还原过程中的离子方程式2IO3-+3N2H4•H2O═3N2+2I-+9H2O;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过100℃;请选择下列试剂检测所得碘化钠固体中是否含有NalO3杂质BD(选填字母).
A.FeCl2溶液 B.冰醋酸
C.CKI溶液 D.淀粉溶液
(3)测定产品中NaI含量的实验步骤如下:
a.称取4.000g 样品、溶解,在250mL 容量瓶中定容;
b.量取25.00ml 待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入A溶液作指示剂;
c.用 0.1000mol•L-1 的Na2S2O3,溶液进行滴定至终点(发生反应的方程式为:
2Na2S2O3+I2═Na2S4O2+2NaI),重复测定2次,所得的相关数据如下表:
①操作b中,加入足量的FeCl3溶液时所发生的离子方程式为2Fe3++2I-═2Fe2++I2.
②加入A物质为淀粉试液(填名称);滴定终点观察到的现象为溶液由浅蓝色褪色,且半分钟内不变色.
③计算该样品中NaI的含量为90%.
(只写出有具体数值的表达式即可)
(4)碘化钠固体的保存方法是密封保存.

已知:N2H4•H2O在100℃以上分解.
(1)已知,在合成过程的反应产物中含有NalO3,则在合成过程中消耗了3mol I2,所生成 NalO3的物质的量为1mol.
(2)写出还原过程中的离子方程式2IO3-+3N2H4•H2O═3N2+2I-+9H2O;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过100℃;请选择下列试剂检测所得碘化钠固体中是否含有NalO3杂质BD(选填字母).
A.FeCl2溶液 B.冰醋酸
C.CKI溶液 D.淀粉溶液
(3)测定产品中NaI含量的实验步骤如下:
a.称取4.000g 样品、溶解,在250mL 容量瓶中定容;
b.量取25.00ml 待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入A溶液作指示剂;
c.用 0.1000mol•L-1 的Na2S2O3,溶液进行滴定至终点(发生反应的方程式为:
2Na2S2O3+I2═Na2S4O2+2NaI),重复测定2次,所得的相关数据如下表:
| 测定 序号 | 待测液体积/mL | 标准液滴定管起点读数/mL | 标准液滴定管终点读数/mL |
| 1 | 25.00 | 0.06 | 24.04 |
| 2 | 25.00 | 0.02 | 24.02 |
| 3 | 25.00 | 0.12 | 24.14 |
②加入A物质为淀粉试液(填名称);滴定终点观察到的现象为溶液由浅蓝色褪色,且半分钟内不变色.
③计算该样品中NaI的含量为90%.
(只写出有具体数值的表达式即可)
(4)碘化钠固体的保存方法是密封保存.
6.乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
已知:
①苯胺易被氧化.
②乙酰苯胺、苯胺和醋酸的部分物理性质如表:
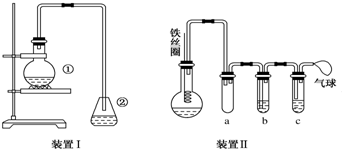
实验步骤如下:
步骤1:在a中,加入9mL (0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,依照图装置组装仪器.
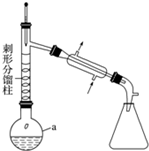
步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全.
步骤3:趁热将反应混合物倒入盛有100mL 冷水的烧杯中,冷却后抽滤、洗涤,得到粗产品.
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g.
请回答下列问题:
(1)仪器a的名称为圆底烧瓶,所选仪器a的最佳规格是B(填序号).
A. 25mL B.50mL C.100mL D.250mL
(2)实验中加入少许锌粉的目的是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中,控制温度计读数在105℃左右的原因是温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出.
(4)判断反应已基本完全的方法为锥形瓶不再有水增加.
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是若让反应混合物冷却,则固体析出沾在瓶壁上不易处理.
(6)步骤4中粗产品进一步提纯,该提纯方法是重结晶.
(7)本次实验的产率为80%.
已知:

①苯胺易被氧化.
②乙酰苯胺、苯胺和醋酸的部分物理性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 乙酰苯胺 | 114.3 | 305 | 微溶于冷水,易溶于热水 |
| 苯胺 | -6 | 184.4 | 微溶于水 |
| 醋酸 | 16.6 | 118 | 易溶于水 |
步骤1:在a中,加入9mL (0.10mol)苯胺、15mL(0.27mol)冰醋酸及少许锌粉,依照图装置组装仪器.

步骤2:控制温度计读数在105℃左右,小火加热回流至反应完全.
步骤3:趁热将反应混合物倒入盛有100mL 冷水的烧杯中,冷却后抽滤、洗涤,得到粗产品.
步骤4:将步骤3所得粗产品进一步提纯后,称得产品质量为10.8g.
请回答下列问题:
(1)仪器a的名称为圆底烧瓶,所选仪器a的最佳规格是B(填序号).
A. 25mL B.50mL C.100mL D.250mL
(2)实验中加入少许锌粉的目的是防止苯胺被氧化,同时起着沸石的作用.
(3)步骤2中,控制温度计读数在105℃左右的原因是温度过低不能蒸出反应所生成的水或温度过高未反应的乙酸蒸出.
(4)判断反应已基本完全的方法为锥形瓶不再有水增加.
(5)步骤3中趁热将混合物倒入盛有冷水的烧杯中,“趁热”的原因是若让反应混合物冷却,则固体析出沾在瓶壁上不易处理.
(6)步骤4中粗产品进一步提纯,该提纯方法是重结晶.
(7)本次实验的产率为80%.
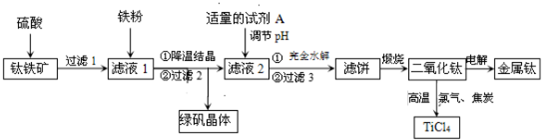
19.碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料.请根据题意回答下列问题:
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
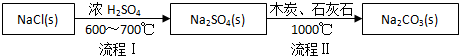
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
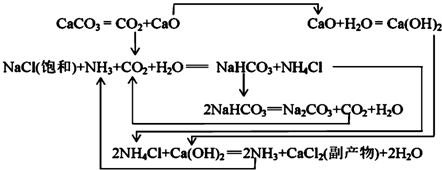
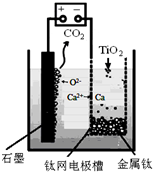
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:
20℃时一些物质在水中的溶解度/g•(100gH2O)-1
(2)氨碱法生成纯碱的原料是食盐、水、氨气和CO2,可循环利用的物质有CaO、CO2、NH4Cl、NH3.
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小、反应消耗水、NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
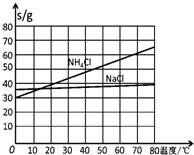
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)
0 159561 159569 159575 159579 159585 159587 159591 159597 159599 159605 159611 159615 159617 159621 159627 159629 159635 159639 159641 159645 159647 159651 159653 159655 159656 159657 159659 159660 159661 159663 159665 159669 159671 159675 159677 159681 159687 159689 159695 159699 159701 159705 159711 159717 159719 159725 159729 159731 159737 159741 159747 159755 203614
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法.其流程如下:
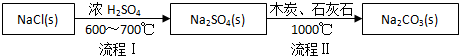
(1)流程I的另一产物是HCl,流程Ⅱ的反应分步进行:a.Na2SO4+4C $\frac{\underline{\;1000℃\;}}{\;}$Na2S+4CO↑;
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为Na2SO4+4C+CaCO3$\frac{\underline{\;1000℃\;}}{\;}$Na2CO3+CaS+4CO↑.
Ⅱ.1862年,比利时人索尔维(Ernest Solvay)用氨碱法生产碳酸钠.反应原理如下:

20℃时一些物质在水中的溶解度/g•(100gH2O)-1
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:反应体系中NaHCO3溶解度最小、反应消耗水、NaHCO3相对分子质量最大.
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原料利用率.
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在0~10℃(填温度范围)下析出NH4Cl.(填化学式)

 .②中离子方程式为Br-+Ag+═AgBr↓.
.②中离子方程式为Br-+Ag+═AgBr↓. 与Br2,要想得到纯净的产物,可用NaOH溶液试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗.
与Br2,要想得到纯净的产物,可用NaOH溶液试剂洗涤.洗涤后分离粗产品应使用的仪器是分液漏斗.