2.用下列方案配制物质的量浓度为0.1mol/L的溶液,其中可行的是( )
| A. | 将4 g NaOH溶解在1L蒸馏水中 | |
| B. | 用托盘天平称量5.85g NaCl固体溶于蒸馏水,配成1000mL溶液 | |
| C. | 常温常压下,将11.2L HCl气体溶于蒸馏水,配成500mL溶液 | |
| D. | 取50 mL 0.5mol/L 的KNO3溶液用蒸馏水稀释,配成250mL 溶液 |
1.为配制0.01mol•L-1 的KMnO4 消毒液,下列操作导致所配溶液浓度偏高的是( )
| A. | 溶解搅拌时有液体飞溅 | |
| B. | 取KMnO4样品时不慎在表面沾了点蒸馏水 | |
| C. | 定容时俯视容量瓶刻度线 | |
| D. | 定容摇匀后见液面下降,再加水至刻度线 |
20.0.3mol的气体高能燃料乙硼烷(B2H6)在O2中燃烧,生成固态B2O3和液态H2O,放出649.5kJ的热量.又知:H2O(l)═H2O(g)△H=+44kJ/mol.下列热化学方程式正确的是( )
| A. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165kJ•mol-1 | |
| B. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ•mol-1 | |
| C. | B2H6(g)+3O2(g)═B2O3+3H2O△H=-2165kJ•mol-1 | |
| D. | B2H6(g)+O2(g)═B2O3(s)+H2O(l)△H=-2165kJ•mol-1 |
18.在一定条件下,发生反应:2X(g)+Y(g)?Z(g)△H=-197kJ•mol-1,若将2mol X和1mol Y充入2L的恒容密闭容器中,反应10min,测得X的物质的量为1.4mol,下列说法正确的是( )
| A. | 10min内,反应放出的热量为197kJ热量 | |
| B. | 10min内,X的平均反应速率为0.06mol•L-1•min-1 | |
| C. | 第10min时,Y的反应速率小于0.015mol•L-1•min-1(假如体系温度不变) | |
| D. | 第10min时,Z浓度为0.6mol•L-1 |
17.某硫酸试剂瓶上的标签如图所示,某同学从瓶中倒出50mL用于配制稀硫酸,求:
(1)50mL该浓硫酸的质量为90.5g,其中含溶质88.69g,物质的量浓度是18.1mol•L-1.
(2)将50mL该浓硫酸与200mL水均匀混合,所得稀硫酸的质量分数是多少?
| 浓硫酸(H2SO4)500mL | |
| 浓度(质量分数) | 98% |
| 密度 | 1.81g•cm-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
(2)将50mL该浓硫酸与200mL水均匀混合,所得稀硫酸的质量分数是多少?
16.七铝十二钙 (12CaO•7Al2O3)是一种新型的超导材料和发光材料,它是用AlC13溶液溶解一定量的CaCO3形成溶液,再用氨水沉淀,然后锻烧沉淀制备.工业上制备AlC13溶液用图示流程(已知A1C13易升华).
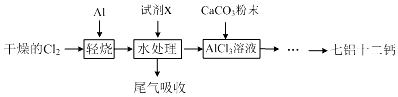
(1)轻烧后的气体用水处理前导气管为何要保温?为了防止AlC13蒸气凝华堵塞导气管
(2)用水处理添加的试剂X是盐酸,其目的是抑制铝离子水解.
(3)AlC13溶液溶解CaCO3时,要控制碳酸钙和AlC13的量,要求n(CaCO3):n(A1C13)>12:14,其原因是氢氧化钙微溶于水,造成损失.用氨水沉淀、过滤后的滤液主要成分是NH4Cl(少量CaCl2).
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12•2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水,加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤.(实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计).
已知:几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
补全实验步骤:向滤液中加盐酸酸化,蒸发浓缩,冷却结晶,过滤冰水洗涤,干燥,得到CaC12•2H2O.

(1)轻烧后的气体用水处理前导气管为何要保温?为了防止AlC13蒸气凝华堵塞导气管
(2)用水处理添加的试剂X是盐酸,其目的是抑制铝离子水解.
(3)AlC13溶液溶解CaCO3时,要控制碳酸钙和AlC13的量,要求n(CaCO3):n(A1C13)>12:14,其原因是氢氧化钙微溶于水,造成损失.用氨水沉淀、过滤后的滤液主要成分是NH4Cl(少量CaCl2).
(4)以工业碳酸钙(含有少量A12O3、Fe3O4杂质)生产二水合氯化钙(CaC12•2H2O)的方法为:将工业碳酸钙溶于盐酸,加入双氧水,加入氢氧化钙,搅拌,用pH计调节溶液的pH为4.7,过滤.(实验中需用到的试剂和仪器有:盐酸,双氧水,氢氧化钙,冰水,pH计).
已知:几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.5 | 4.7 |
15.实验室里需要配制180mL1mol•L-1SrCl2溶液,下列实验用品及实验操作都正确的是( )
0 159551 159559 159565 159569 159575 159577 159581 159587 159589 159595 159601 159605 159607 159611 159617 159619 159625 159629 159631 159635 159637 159641 159643 159645 159646 159647 159649 159650 159651 159653 159655 159659 159661 159665 159667 159671 159677 159679 159685 159689 159691 159695 159701 159707 159709 159715 159719 159721 159727 159731 159737 159745 203614
| 选项 | 容量瓶容积 | 固体质量 | 实验操作 |
| A | 180mL | SrCl2:28.6g | 加入180mL水 |
| B | 200mL | SrCl2:31.8g | 配成200mL溶液 |
| C | 250mL | SrCl2:39.8g | 配成250mL溶液 |
| D | 250mL | SrCl2•2H2O:39.8g | 配成250mL溶液 |
| A. | A | B. | B | C. | C | D. | D |
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):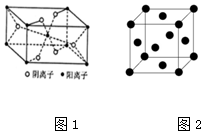 W、X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;W是形成有机物种类最多的元素;R2+的3d轨道中有9个电子.请回答:
W、X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;W是形成有机物种类最多的元素;R2+的3d轨道中有9个电子.请回答: