2.2013年中国已超北美成为全球液晶显示器第二大市场.生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
下列说法中不正确的是( )
| 化学键 | N≡N | F-F | N-F |
| 键能:kJ/mol | 941.7 | 154.8 | 283.0 |
| A. | 过程F2(g)→2F(g)吸收能量 | |
| B. | 过程N(g)+3F(g)→NF3(g) 放出能量 | |
| C. | 反应N2(g)+3F2(g)=2NF3(g) 放出能量 | |
| D. | NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
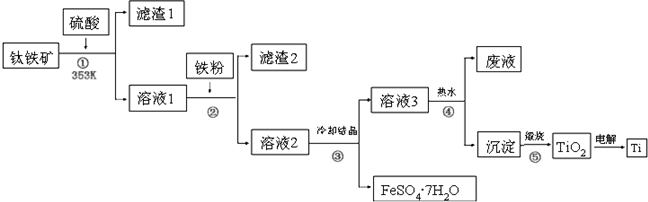
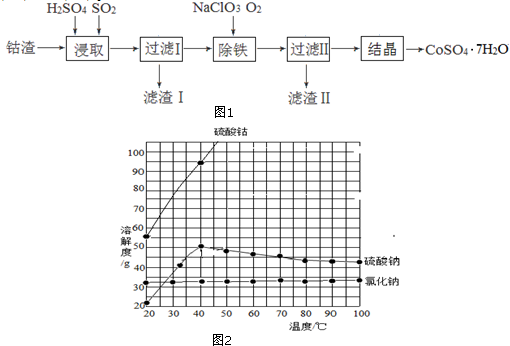
20.工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取KMnO4.其流程示意图如下:

②金属阳离子生成氢氧化物沉淀的pH如下表:
回答下列问题:
(1)写出滤渣1的一种工业用途:建筑材料.实验室模拟该流程过程中,洗涤滤渣1的具体操作方法为将沉淀放在过滤器中,水浸没沉淀自然流下,重复2~3次.
(2)试剂a最好选用B(填选项字母).
A.氯水 B.高锰酸钾
C.次氯酸钠 D.浓盐酸
(3)试剂b可选用CD(填选项字母).
A.氨水 B.稀硫酸 C.碳酸锰 D.Mn(OH)2 E.NaOH
(4)试剂c为MnS,写出滤液2中加入MnS后发生反应的离子方程式:MnS+Cu2+=Mn2++CuS
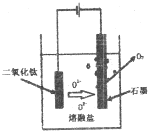
(5)用惰性电极电解硫酸锰和硫酸钾混合溶液的方法可以制取高锰酸钾,写出电解时的阳极反应式:Mn2+-5e-+4H2O=8H++MnO4-.工业上用硫酸溶解碳酸锰,而不用盐酸溶解,其原因是氯离子放电生成有毒气体氯气.
(6)KMnO4是一种常用的滴定试剂,某同学用酸性高锰酸钾溶液测定滤液1中Fe2+的含量.滴定过程中,每次均量取25.00mL的滤液1置于锥形瓶中,滴定三次平均消耗掉0.1000mol/L的KMnO4溶液20.00mL,则滤液1中Fe2+的浓度为22.4g/L(保留三位有效数字).

②金属阳离子生成氢氧化物沉淀的pH如下表:
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉定时 | 8.3 | 7.6 | 2.7 | 6.7 |
| 完全沉淀时 | 9.8 | 9.6 | 3.7 | 9 |
(1)写出滤渣1的一种工业用途:建筑材料.实验室模拟该流程过程中,洗涤滤渣1的具体操作方法为将沉淀放在过滤器中,水浸没沉淀自然流下,重复2~3次.
(2)试剂a最好选用B(填选项字母).
A.氯水 B.高锰酸钾
C.次氯酸钠 D.浓盐酸
(3)试剂b可选用CD(填选项字母).
A.氨水 B.稀硫酸 C.碳酸锰 D.Mn(OH)2 E.NaOH
(4)试剂c为MnS,写出滤液2中加入MnS后发生反应的离子方程式:MnS+Cu2+=Mn2++CuS
(5)用惰性电极电解硫酸锰和硫酸钾混合溶液的方法可以制取高锰酸钾,写出电解时的阳极反应式:Mn2+-5e-+4H2O=8H++MnO4-.工业上用硫酸溶解碳酸锰,而不用盐酸溶解,其原因是氯离子放电生成有毒气体氯气.
(6)KMnO4是一种常用的滴定试剂,某同学用酸性高锰酸钾溶液测定滤液1中Fe2+的含量.滴定过程中,每次均量取25.00mL的滤液1置于锥形瓶中,滴定三次平均消耗掉0.1000mol/L的KMnO4溶液20.00mL,则滤液1中Fe2+的浓度为22.4g/L(保留三位有效数字).
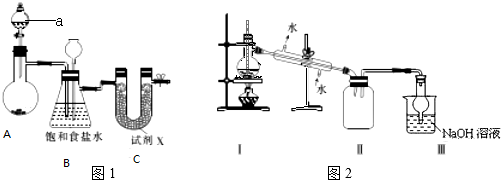
19.硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得. 已知:Na2S2O3在酸性溶液中不能稳定存在.
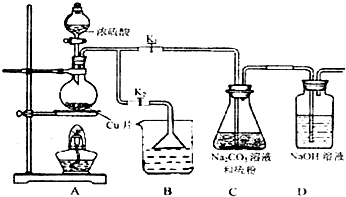
(1)某研究小组设计了制备Na2S203•5H20装置和部分操作步骤如下.
I.打开K1关闭K2,向圆底 烧瓶中加入足量浓硫酸加热.
II.C中混合液被气流搅动,反应一段时间后,硫粉逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热.
III.过滤C中的混合液.
IV.将滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、烘干,得到产品Na2S203.5H20.
回答下列问题:
①II中,“当C中溶液的pH接近7时即停止C中的反应”的原因S2O32-+2H+═S↓+SO2↑+H2O(用离子方程式表示).
②IV中,操作步骤是蒸发浓缩、冷却结晶.
③装置B中盛放的试剂是(填化学式)NaOH溶液.
(2)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO${\;}_{4}^{2-}$全部转化为Cr2O${\;}_{7}^{2-}$;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.0010mol.L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
部分反应离子方程式为:
①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O;
②I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$.
Ⅰ.判断达到滴定终点的现象是加入最后一滴Na2S2O3标准溶液后,蓝色消失,且半分钟内颜色不改变
Ⅱ.从表格所给数据计算:一份待测溶液消耗Na2S2O3溶液的平均体积为18.00 ml
Ⅲ.废水中Ba2+的物质的量浓度2.4×10-4mol•L-1.

(1)某研究小组设计了制备Na2S203•5H20装置和部分操作步骤如下.
I.打开K1关闭K2,向圆底 烧瓶中加入足量浓硫酸加热.
II.C中混合液被气流搅动,反应一段时间后,硫粉逐渐减少,当C中溶液的pH 接近7时,打开K2,关闭K1即停止C中的反应,停止加热.
III.过滤C中的混合液.
IV.将滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、烘干,得到产品Na2S203.5H20.
回答下列问题:
①II中,“当C中溶液的pH接近7时即停止C中的反应”的原因S2O32-+2H+═S↓+SO2↑+H2O(用离子方程式表示).
②IV中,操作步骤是蒸发浓缩、冷却结晶.
③装置B中盛放的试剂是(填化学式)NaOH溶液.
(2)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量 K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO${\;}_{4}^{2-}$全部转化为Cr2O${\;}_{7}^{2-}$;再加过KI溶液,充分反应后得混合溶液V mL,将其平均分成4等份,加入淀粉溶液作指示剂,用0.0010mol.L-1 的Na2S2O3溶液进行滴定,反应完全时,相关数据记录如表所示:
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O;
②I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$.
Ⅰ.判断达到滴定终点的现象是加入最后一滴Na2S2O3标准溶液后,蓝色消失,且半分钟内颜色不改变
Ⅱ.从表格所给数据计算:一份待测溶液消耗Na2S2O3溶液的平均体积为18.00 ml
Ⅲ.废水中Ba2+的物质的量浓度2.4×10-4mol•L-1.
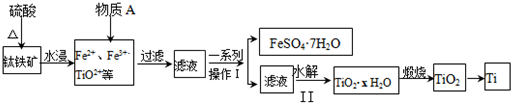
14.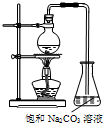 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、纺织等工业.乙酸乙酯的实验室和工业制法如下:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、纺织等工业.乙酸乙酯的实验室和工业制法如下:
CH3COOH+C2H5OH$\frac{\underline{\;浓硫酸\;}}{△}$CH3COOC2H5+H2O
回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有(答出2点即可):增大乙醇浓度、移去生成物等.
(2)若用如图所示装置制备乙酸乙酯,产率往往偏低.其原因是(答出2点即可):原料来不及反应就被蒸出,或温度过高发生副反应;
(3)此反应以浓硫酸为催化剂,可能会造成(答出2点即可)产生大量酸性废液污染环境,或部分原料炭化等问题.
(4)目前对催化剂进行研究,发现质子酸(能提供H+)离子液体可用作此反应的催化剂,且能重复使用.实验数据如下(乙酸和乙醇等物质的量):
①根据表中数据,该反应的最佳条件是C.
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
②当反应达到120℃时,反应选择性降低的原因可能是:乙醇脱水生成乙醚.
0 159543 159551 159557 159561 159567 159569 159573 159579 159581 159587 159593 159597 159599 159603 159609 159611 159617 159621 159623 159627 159629 159633 159635 159637 159638 159639 159641 159642 159643 159645 159647 159651 159653 159657 159659 159663 159669 159671 159677 159681 159683 159687 159693 159699 159701 159707 159711 159713 159719 159723 159729 159737 203614
 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、纺织等工业.乙酸乙酯的实验室和工业制法如下:
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、纺织等工业.乙酸乙酯的实验室和工业制法如下:CH3COOH+C2H5OH$\frac{\underline{\;浓硫酸\;}}{△}$CH3COOC2H5+H2O
回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有(答出2点即可):增大乙醇浓度、移去生成物等.
(2)若用如图所示装置制备乙酸乙酯,产率往往偏低.其原因是(答出2点即可):原料来不及反应就被蒸出,或温度过高发生副反应;
(3)此反应以浓硫酸为催化剂,可能会造成(答出2点即可)产生大量酸性废液污染环境,或部分原料炭化等问题.
(4)目前对催化剂进行研究,发现质子酸(能提供H+)离子液体可用作此反应的催化剂,且能重复使用.实验数据如下(乙酸和乙醇等物质的量):
| 同一反应时间 | 同一反应温度 | ||||
| 反应温度 | 转化率(%) | 选择性(%) | 反应时间 | 转化率(%) | 选择性(%) |
| 40℃ | 77.8 | 100 | 2h | 80.2 | 100 |
| 60℃ | 92.3 | 100 | 3h | 87.8 | 100 |
| 80℃ | 92.6 | 100 | 4h | 92.3 | 100 |
| 120℃ | 94.5 | 98.7 | 6h | 93 | 100 |
| 注:选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
A.120℃,4h B.80℃,2h C.60℃,4h D.40℃,3h
②当反应达到120℃时,反应选择性降低的原因可能是:乙醇脱水生成乙醚.
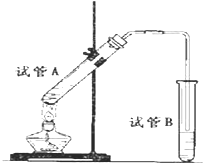 如图所示,中学化学实验室采用该装置用于制备乙酸乙酯.
如图所示,中学化学实验室采用该装置用于制备乙酸乙酯.