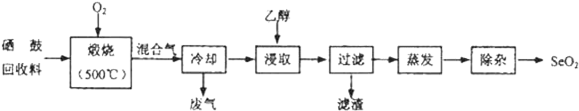
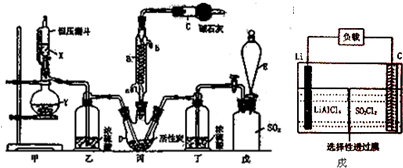
7.硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):
部分物质的物理性质如表:
回答下列问题:
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为第四周期ⅥA族;H2Se的热稳定性比H2S的热稳定性弱(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是升华.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式H2SeO3+4HI=Se↓+2I2+3H2O.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈碱性,原因是(用离子方程式表示)SeO32-+H2O?HSeO3-+OH-;
②在Na2SeO3溶液中,下列关系式正确的是C:
A.c(Na+)+c(H+)═c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)═c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)═2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)═c(H+)+c(HSeO3-)+c(H2SeO3)

部分物质的物理性质如表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为第四周期ⅥA族;H2Se的热稳定性比H2S的热稳定性弱(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是升华.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式H2SeO3+4HI=Se↓+2I2+3H2O.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈碱性,原因是(用离子方程式表示)SeO32-+H2O?HSeO3-+OH-;
②在Na2SeO3溶液中,下列关系式正确的是C:
A.c(Na+)+c(H+)═c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)═c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)═2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)═c(H+)+c(HSeO3-)+c(H2SeO3)
1.2-硝基-l,3-苯二酚由间苯二酚先磺化,再硝化,后去磺酸基生成.原理如下:
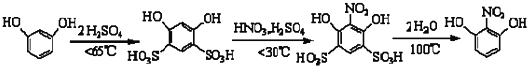
部分物质的相关性质如下:
制备过程如下:第一步:磺化.称取 71.5g间苯二酚,碾成粉末放入烧瓶中,慢慢加入适量浓硫酸并不断搅拌,控制温度在一定范围内 15min(如图 1).
第二步:硝化.待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温度继续搅拌 l 5min.
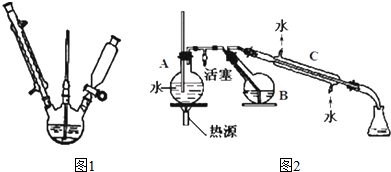
第三步:蒸馏.将硝化反应混物的稀释液转移到圆底烧瓶 B中,然后用图 2所示装置进行水 蒸气蒸馏.
请回答下列问题:
(1)实验室中把问苯二酚碾成粉末需要的仪器是研钵.
(2)磺化步骤中控制温度最合适的范围为(填字母)B.
A.30℃~60℃B.60℃~65℃C.65℃~70℃D.70℃~100℃
(3)硝化步骤中制取“混酸”的具体操作是在锥形瓶中加适量的浓硝酸,在摇荡下缓慢加入一定量的浓硫酸,冷却.
(4)图 2 中,烧瓶 A 中长玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能防止压强过小产生倒吸;直形冷凝管 C中可能出现的现象是有桔红色晶体析出.
(5)水蒸气蒸馏是分离和提纯有机物的方法之一,被提纯物质必须具备的条件正确的abc.
a.不溶或难溶于水,便于最后分离 b.在沸腾下与水不发生化学反应
c.具有一定的挥发性 d.具有较低的熔点
(6)本实验最终获得 12.0g桔红色晶体,则 2-硝基-1,3-苯二酚的产率约为11.9%.
部分物质的相关性质如下:
| 名称 | 相对分子质量 | 性状 | 熔点 | 水溶性(常温) |
| 间苯二酚 | 110 | 白色针状晶体 | 110.7 | 易容 |
| 2-硝基-1,3-苯二酚 | 155 | 桔红色针状晶体 | 87.8 | 难溶 |
第二步:硝化.待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温度继续搅拌 l 5min.

第三步:蒸馏.将硝化反应混物的稀释液转移到圆底烧瓶 B中,然后用图 2所示装置进行水 蒸气蒸馏.
请回答下列问题:
(1)实验室中把问苯二酚碾成粉末需要的仪器是研钵.
(2)磺化步骤中控制温度最合适的范围为(填字母)B.
A.30℃~60℃B.60℃~65℃C.65℃~70℃D.70℃~100℃
(3)硝化步骤中制取“混酸”的具体操作是在锥形瓶中加适量的浓硝酸,在摇荡下缓慢加入一定量的浓硫酸,冷却.
(4)图 2 中,烧瓶 A 中长玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能防止压强过小产生倒吸;直形冷凝管 C中可能出现的现象是有桔红色晶体析出.
(5)水蒸气蒸馏是分离和提纯有机物的方法之一,被提纯物质必须具备的条件正确的abc.
a.不溶或难溶于水,便于最后分离 b.在沸腾下与水不发生化学反应
c.具有一定的挥发性 d.具有较低的熔点
(6)本实验最终获得 12.0g桔红色晶体,则 2-硝基-1,3-苯二酚的产率约为11.9%.
20. 苯甲醛(
苯甲醛(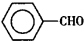 )、苯甲酸(
)、苯甲酸(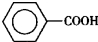 )都是重要的化工原料,都可用甲苯(
)都是重要的化工原料,都可用甲苯(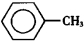 )为原料生产.下表列出了有关物质的部分物理性质,请回答:
)为原料生产.下表列出了有关物质的部分物理性质,请回答:
注:甲苯、苯甲醛、苯甲酸三者互溶.
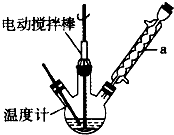
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)仪器a的主要作用是冷凝回流,防止甲苯挥发导致产率降低.三颈瓶中发生反应的化学方程式为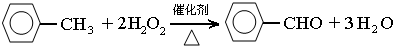 .
.
(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是温度过高时过氧化氢分解速度加快,实际参加反应的过氧化氢质量减小,影响产量.
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2 d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于100mL乙醇配成溶液,量取所得的乙醇溶液10.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/LKOH标准液滴定,到达滴定终点时消耗KOH溶液20.00mL.产品中苯甲酸的质量分数为97.60%.下列情况会使测定结果偏低的是ad(填字母).
a.滴定时俯视读取耗碱量 b.碱式滴定管用蒸馏水洗净后即盛装KOH标准液
c.配制KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液.
0 159529 159537 159543 159547 159553 159555 159559 159565 159567 159573 159579 159583 159585 159589 159595 159597 159603 159607 159609 159613 159615 159619 159621 159623 159624 159625 159627 159628 159629 159631 159633 159637 159639 159643 159645 159649 159655 159657 159663 159667 159669 159673 159679 159685 159687 159693 159697 159699 159705 159709 159715 159723 203614
 苯甲醛(
苯甲醛( )、苯甲酸(
)、苯甲酸( )都是重要的化工原料,都可用甲苯(
)都是重要的化工原料,都可用甲苯( )为原料生产.下表列出了有关物质的部分物理性质,请回答:
)为原料生产.下表列出了有关物质的部分物理性质,请回答:| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 ρ水=1g/cm3 | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)仪器a的主要作用是冷凝回流,防止甲苯挥发导致产率降低.三颈瓶中发生反应的化学方程式为
 .
.(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是温度过高时过氧化氢分解速度加快,实际参加反应的过氧化氢质量减小,影响产量.
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2 d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于100mL乙醇配成溶液,量取所得的乙醇溶液10.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/LKOH标准液滴定,到达滴定终点时消耗KOH溶液20.00mL.产品中苯甲酸的质量分数为97.60%.下列情况会使测定结果偏低的是ad(填字母).
a.滴定时俯视读取耗碱量 b.碱式滴定管用蒸馏水洗净后即盛装KOH标准液
c.配制KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液.


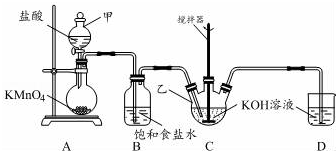 实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.
实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4.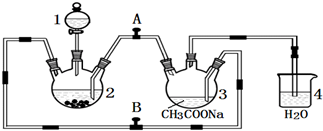
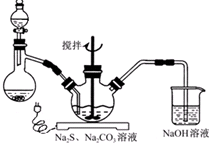 NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题:
NaCN为剧毒无机物.某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题: