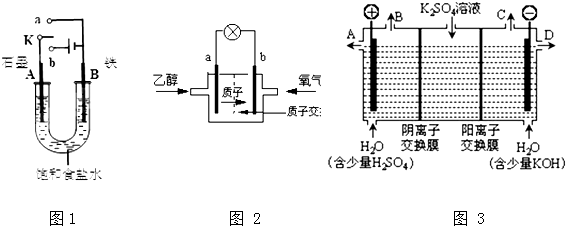
13.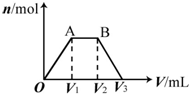 有KOH和Ca(OH)2的混合溶液,pH=13.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
有KOH和Ca(OH)2的混合溶液,pH=13.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
 有KOH和Ca(OH)2的混合溶液,pH=13.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
有KOH和Ca(OH)2的混合溶液,pH=13.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )| A. | 560、672 | B. | 1008、1120 | C. | 2240、2352 | D. | 392、504 |
12.工业制备氯化铜时,将浓盐酸加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤.请回答以下问题:
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
(1)将浓盐酸溶解粗CuO粉末后,溶液中的金属阳离子含有Cu2+、Fe2+、Fe3+、H+,第一步除去该溶液中的Fe2+,能否直接调整溶液pH=9.6,将Fe2+沉淀除去?不能,(填“能”或“不能”)理由是因Fe2+沉淀的pH最大,Fe2+沉淀完全时,Cu2+、Fe3+也会沉淀完全
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?否(填“是”或“否”),现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有BD(有几个选几个,填代号,下同).
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的AD.
A.CuO B.NH3•H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的PH为3.2~4.7,原因是铁离子沉淀完全时的PH值为3.2,铜离子开始沉淀时的PH值为4.7,除杂时要使铁离子沉淀完全,不能使铜离子产生沉淀
(4)最后能不能直接将溶液蒸发得到CuCl2•2H2O?不能(填“能”或者“不能”).若不能,应该如何操作才能得到CuCl2•2H2O应在氯化氢气氛中浓缩后冷却结晶(若填“能”,此空不用回答)
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9 | 6.7 |
(2)有人用强氧化剂NaClO先将Fe2+氧化为Fe3+,再调整溶液的PH将Fe3+沉淀除去:你认为用NaClO作氧化剂是否妥当?否(填“是”或“否”),现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有BD(有几个选几个,填代号,下同).
A.浓HNO3 B.Cl2 C.KMnO4 D.H2O2
(3)①加入适当物质调整溶液pH,使Fe3+转化为Fe(OH)3沉淀,可以达到除去Fe3+而不损失CuCl2的目的,则调整溶液pH可选用下列物质中的AD.
A.CuO B.NH3•H2O C.NaOH D.Cu(OH)2
②加上述物质调节溶液的PH为3.2~4.7,原因是铁离子沉淀完全时的PH值为3.2,铜离子开始沉淀时的PH值为4.7,除杂时要使铁离子沉淀完全,不能使铜离子产生沉淀
(4)最后能不能直接将溶液蒸发得到CuCl2•2H2O?不能(填“能”或者“不能”).若不能,应该如何操作才能得到CuCl2•2H2O应在氯化氢气氛中浓缩后冷却结晶(若填“能”,此空不用回答)
9.下列说法不正确的是( )
| A. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 叠氮酸(HN3)与醋酸酸性相似,NaN3水溶液中离子浓度大小顺序为c(Na+)>c(N3-)>c(OH-)>c(H+) | |
| C. | 常温下向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中c(NH4+)=c(Cl-) | |
| D. | 常温下,等pH的CH3COONa、NaHCO3、NaClO三种溶液的浓度大小关系为c(NaClO)>c(NaHCO3)>c(CH3COONa) |
8.用惰性电极电解100mL含c(H+)=0.30mol•L-1下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是( )
| A. | 0.10 mol•L-1AgNO3溶液 | B. | 0.10 mol•L-1ZnSO4溶液 | ||
| C. | 0.20 mol•L-1CuCl2溶液 | D. | 0.20 mol•L-1Mg(NO3)2溶液 |
7.用惰性电极电解下列电解质溶液,有关叙述正确的是( )
| A. | 等物质的量浓度的NaCl和AlCl3混合液完全电解后,所得的混合液的pH值增大 | |
| B. | NaCl溶液电解一定时间后,要恢复到电解前状态,应加入适量盐酸 | |
| C. | Na2SO4溶液在电解过程中,阴极区pH值降低 | |
| D. | 电解CuSO4溶液,阳极反应式为:2H2O+O2+4e-=4OH- |
6.常温下,在10mL 0.01mol/L的NaOH溶液中,加入10mL某酸,再滴入紫色石蕊试液,溶液显红色,这种酸可能是( )
| A. | 0.01mol/L CH3COOH溶液 | B. | 0.01mol/L HNO3溶液 | ||
| C. | pH=2的H2SO4溶液 | D. | pH=2的CH3COOH溶液 |
5.下列各组离子能在指定环境下大量共存的是( )
| A. | C(HCO3-)=0.1mol/L的溶液中:NH4+、Al3+、Cl-、NO3- | |
| B. | 室温下,PH=2的溶液中:Fe2+、SO42-、Na+、NO3- | |
| C. | 无色透明的溶液中:NH4+、Cl-、NO3-、Fe3+ | |
| D. | 使红色石蕊试纸变蓝的溶液中:SO32-、Na+、CO32-、K+ |
4.反应速率v和反应物浓度的关系是用实验方法测定的,化学反应:H2+Cl2=2HCl的反应速率v可表示为:v=k[c(H2)]m•[c(Cl2)]n,k为常数,m,n值可用表中的数据确定
由此可推断m,n值正确的是( )
0 159499 159507 159513 159517 159523 159525 159529 159535 159537 159543 159549 159553 159555 159559 159565 159567 159573 159577 159579 159583 159585 159589 159591 159593 159594 159595 159597 159598 159599 159601 159603 159607 159609 159613 159615 159619 159625 159627 159633 159637 159639 159643 159649 159655 159657 159663 159667 159669 159675 159679 159685 159693 203614
| v(mol•L-1•s-1) | c(H2)(mol•L-1) | c(Cl2)(mol•L-1) |
| 1.0k | 1.0 | 1.0 |
| 2.0k | 2.0 | 1.0 |
| 4.0k | 2.0 | 4.0 |
| A. | m=1,n=1 | B. | m=$\frac{1}{2}$,n=$\frac{1}{2}$ | C. | m=$\frac{1}{2}$,n=1 | D. | m=1,n=$\frac{1}{2}$ |