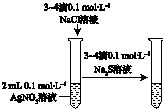
9.下列说法正确的是( )
| A. | 红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 | |
| B. | 石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 | |
| C. | 氢氧燃料电池、丹尼尔电池、硅太阳能电池中都利用了原电池原理 | |
| D. | 纤维素、PLA、纤维二糖、甲壳素、硝化纤维等都是高分子化合物 |
7.一种新型净水剂PAFC(聚合氯化铁铝,化学式可表示为[AlFe(OH)nCl6-n]m,n<5,m<10),广泛用于生活用水的净化和废水的净化.下列有关PAFC的说法正确的是( )
| A. | PAFC用于净化饮用水时,比用相同量的氯化铝或氯化铁对水的pH改变大 | |
| B. | PAFC中铁为+2价 | |
| C. | PAFC可看作一定比例的氯化铝和氯化铁的水解产物 | |
| D. | PAFC在强酸性或强碱性溶液中都能稳定存在 |
6.在一次重大车祸事故中,有一人双腿骨折,医生将他受伤较重的膝关节用人造骨骼代替,下列可用作人造关节且利用的性质正确的是( )
| A. | 氮化硅陶瓷 耐高温 | B. | 氧化锆陶瓷 韧性和耐磨性 | ||
| C. | 钛酸钡陶瓷 导电性 | D. | 氧化铝陶瓷 透光性 |
5.下列各种物质不属于新型无机非金属材料的是( )
| A. | 水泥 | B. | 氮化硅陶瓷 | C. | 磷酸钙陶瓷 | D. | 氧化铝陶瓷 |
4.水晶是重要的首饰用品,其主要成分是SiO2,下列有关SiO2的说法正确的是( )
0 159459 159467 159473 159477 159483 159485 159489 159495 159497 159503 159509 159513 159515 159519 159525 159527 159533 159537 159539 159543 159545 159549 159551 159553 159554 159555 159557 159558 159559 159561 159563 159567 159569 159573 159575 159579 159585 159587 159593 159597 159599 159603 159609 159615 159617 159623 159627 159629 159635 159639 159645 159653 203614
| A. | 水晶能溶于水生成H2SiO3 | |
| B. | SiO2是酸性氧化物,不能与任何酸反应 | |
| C. | SiO2既能溶于NaOH溶液,又能溶于HF,因此属于两性氧化物 | |
| D. | SiO2对应的H2SiO3是一种弱酸,酸性比碳酸还弱 |
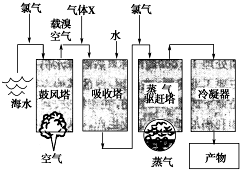 如图所示是以海水为原料,获得某产物的工艺流程图.已知在吸收塔中,溶液的pH显著减小.请回答下列问题:
如图所示是以海水为原料,获得某产物的工艺流程图.已知在吸收塔中,溶液的pH显著减小.请回答下列问题: 如图的框图是利用海水和海边贝壳为原料设计的制备漂白粉的工艺流程.分析图示各物质的关系,然后回答问题.
如图的框图是利用海水和海边贝壳为原料设计的制备漂白粉的工艺流程.分析图示各物质的关系,然后回答问题.