3.6g铁粉,与标况下3.36L氯气充分反应,理论上最多可以得到氯化铁的质量是( )
| A. | 16.25 | B. | 17.41 | C. | 15.51 | D. | 17.10 |
2.在2KMnO4+16HCl=2MnCl2+5Cl2↑+8H2O+2KCl的反应中,氧化剂和还原剂物质的量之比是( )
| A. | 1:8 | B. | 8:1 | C. | 1:5 | D. | 5:1 |
1.向100mL 6mol•L-1 KMnO4溶液中滴加适量稀硫酸,向溶液中缓缓通入5.6L(标准状况)C2H4,恰好完全反应(C2H4中-2价的碱全部转化成CO2),则还原产物中锰元素的化合价为( )
| A. | +6 | B. | +4 | C. | +3 | D. | +2 |
19.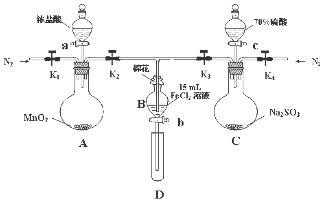 为了验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
为了验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中继续通入N2,然后关闭K1、K3、K4
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
IV.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)棉花中浸润的溶液化学式为NaOH溶液.
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)过程Ⅳ中检验其中Fe3+ 和Fe2+的试剂分别为KSCN溶液和铁氰化钾(或K3[FeCN6])溶液.若确定有Fe3+ 和Fe2+,则现象分别是溶液变红和产生蓝色沉淀.
(5)过程Ⅵ,检验B溶液中含有SO42-的操作是.
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2>Fe3+>SO2的是乙、丙(填“甲”“乙”“丙”).
 为了验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).
为了验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验).实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中继续通入N2,然后关闭K1、K3、K4
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热.
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2.
IV.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子.
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3.
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子.
(1)过程Ⅰ的目的是排出装置中的空气,防止干扰.
(2)棉花中浸润的溶液化学式为NaOH溶液.
(3)A中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(4)过程Ⅳ中检验其中Fe3+ 和Fe2+的试剂分别为KSCN溶液和铁氰化钾(或K3[FeCN6])溶液.若确定有Fe3+ 和Fe2+,则现象分别是溶液变红和产生蓝色沉淀.
(5)过程Ⅵ,检验B溶液中含有SO42-的操作是.
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2>Fe3+>SO2的是乙、丙(填“甲”“乙”“丙”).
| 过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
17.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 18 g D2O和18 g H2O中含有的质子数均为10NA | |
| B. | 1 mol Cu和2mol热的浓硫酸反应可生成NA个SO2分子 | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 |
16.已知C、N、S都是重要的非金属元素.下列说法正确的是( )
0 159373 159381 159387 159391 159397 159399 159403 159409 159411 159417 159423 159427 159429 159433 159439 159441 159447 159451 159453 159457 159459 159463 159465 159467 159468 159469 159471 159472 159473 159475 159477 159481 159483 159487 159489 159493 159499 159501 159507 159511 159513 159517 159523 159529 159531 159537 159541 159543 159549 159553 159559 159567 203614
| A. | 三者的单质直接与O2反应都能生成两种以上的氧化物 | |
| B. | CO2、NO2、SO2都能与H2O发生化合反应 | |
| C. | CO2、NO2、SO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 三种元素在自然界中既有游离态又有化合态 |
