5.为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )


| A. | 现象①③说明物质燃烧需要达到一定的温度 | |
| B. | 现象②③说明物质燃烧需要氧气 | |
| C. | 现象①②说明白磷的着火点比红磷的着火点低 | |
| D. | 现象②说明红磷不是可燃物 |
3.已知在25℃、101kPa下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40kJ热量,表示上述反应的热化学方程式正确的是( )
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O△H=-48.40 kJ/mol | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5518 kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5518 kJ/mol | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+48.40 kJ/mol |
19.下列说法正确的是( )
| A. | 热化学方程式C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(g)△H=-1256kJ/mol,表示乙炔的燃烧热为1256kJ/mol | |
| B. | -OH与OH-组成元素相同,含有的电子数也相同 | |
| C. | H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ/mol,表示含1molNaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 | |
| D. | 中和热测定实验中,不能用铜丝搅拌棒代替环形玻璃搅拌棒 |
18.下列说法正确的是( )
0 159357 159365 159371 159375 159381 159383 159387 159393 159395 159401 159407 159411 159413 159417 159423 159425 159431 159435 159437 159441 159443 159447 159449 159451 159452 159453 159455 159456 159457 159459 159461 159465 159467 159471 159473 159477 159483 159485 159491 159495 159497 159501 159507 159513 159515 159521 159525 159527 159533 159537 159543 159551 203614
| A. | CH3CH2OH和CH3OCH3互为同分异构体 | |
| B. | 原子核内有8个中子的氧原子:${\;}_6^{14}C$ | |
| C. | CH3CH2CH2CH3的一氯代烃只有一种 | |
| D. | CO2的结构式:O-C-O |
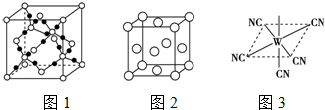
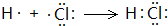 ,
,