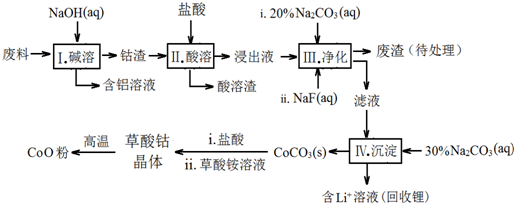
15.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质).
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15.废渣中的成分有LiF,Fe(OH)3.
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2.
(6)某锂离子电池的总反应为C+LiCoO2$?_{放电}^{充电}$ LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)写出步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15.废渣中的成分有LiF,Fe(OH)3.
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2.
(6)某锂离子电池的总反应为C+LiCoO2$?_{放电}^{充电}$ LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
14.某兴趣小组在实验室用加热乙醇、浓H2SO4、溴化钠和少量水的混合物来制备溴乙烷.
反应如下:NaBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
该兴趣小组要通过该实验检验反应的部分副产物,并探究溴乙烷的性质.
乙醇、溴乙烷和溴的有关数据见表:
(一)溴乙烷的制备及产物的检验:设计了如图1装置,其中夹持仪器、加热仪器及冷却水管没有画出.
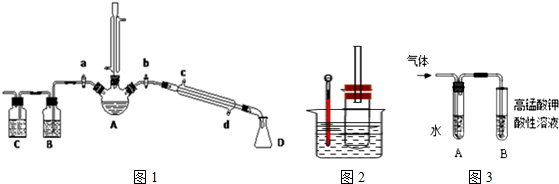
请根据实验步骤,回答下列问题:
(1)三颈烧瓶A上竖直冷凝管冷凝水流向下口进上口出;竖直冷凝管冷凝的作用冷凝回流
(2)反应时若温度过高三颈烧瓶A可看到有红棕色气体产生,该气体的化学式Br2;为了更好的控制反应温度,应采取的加热方式是水浴加热.
(3)理论上,上述反应的副产物还可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氢等.检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验.
B、C中应盛放的试剂分别是四氯化碳、硝酸银溶液.
(4)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是A.(填字母)
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行蒸馏(填操作名称).
(二)溴乙烷性质的探究:
用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:
Ⅰ:在试管中加入10mL6mol/L NaOH溶液和2mL 溴乙烷,振荡.
II:将试管如图2固定后,水浴加热.
(5)观察到液体不分层现象时,表明溴乙烷与NaOH溶液已完全反应.
(6)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,将生成的气体通入如图3装置.A试管中的水的作用是吸收乙醇,若无A试管,B试管中的试剂应为溴水.
反应如下:NaBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
该兴趣小组要通过该实验检验反应的部分副产物,并探究溴乙烷的性质.
乙醇、溴乙烷和溴的有关数据见表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |

请根据实验步骤,回答下列问题:
(1)三颈烧瓶A上竖直冷凝管冷凝水流向下口进上口出;竖直冷凝管冷凝的作用冷凝回流
(2)反应时若温度过高三颈烧瓶A可看到有红棕色气体产生,该气体的化学式Br2;为了更好的控制反应温度,应采取的加热方式是水浴加热.
(3)理论上,上述反应的副产物还可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、溴化氢等.检验副产物中是否含有溴化氢:熄灭酒精灯,在竖直冷凝管上方塞上塞子、打开a,利用余热继续反应直至冷却,通过B、C装置检验.
B、C中应盛放的试剂分别是四氯化碳、硝酸银溶液.
(4)欲除去溴乙烷中的少量杂质Br2,下列物质中最适合的是A.(填字母)
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行蒸馏(填操作名称).
(二)溴乙烷性质的探究:
用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:
Ⅰ:在试管中加入10mL6mol/L NaOH溶液和2mL 溴乙烷,振荡.
II:将试管如图2固定后,水浴加热.
(5)观察到液体不分层现象时,表明溴乙烷与NaOH溶液已完全反应.
(6)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,将生成的气体通入如图3装置.A试管中的水的作用是吸收乙醇,若无A试管,B试管中的试剂应为溴水.
11.下列说法正确的是( )
0 159352 159360 159366 159370 159376 159378 159382 159388 159390 159396 159402 159406 159408 159412 159418 159420 159426 159430 159432 159436 159438 159442 159444 159446 159447 159448 159450 159451 159452 159454 159456 159460 159462 159466 159468 159472 159478 159480 159486 159490 159492 159496 159502 159508 159510 159516 159520 159522 159528 159532 159538 159546 203614
| A. | 焓减小的反应通常是自发的,能够自发进行的反应都是焓减小的反应 | |
| B. | 熵增加的反应通常是自发的,能够自发进行的反应都是熵增加的反应 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g)不能自发进行,则该反应的△H>0 | |
| D. | △H<0且△S<0的反应一定能自发发生 |

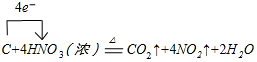 .
.

 x/m,该反应可用来检验Cr2O72-的存在.写出反应的离子方程式Cr2O72-+4H2O2+2H+=2CrO5+5H2O.
x/m,该反应可用来检验Cr2O72-的存在.写出反应的离子方程式Cr2O72-+4H2O2+2H+=2CrO5+5H2O.
 ,其阴阳离子个数比为1:2.
,其阴阳离子个数比为1:2.