1.观察下列几个装置示意图,有关叙述正确的是( )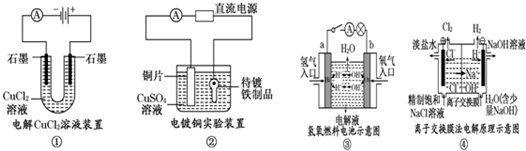

| A. | 装置①中阳极上析出红色固体 | |
| B. | 装置②的待镀铁制品应与电源负极相连 | |
| C. | 装置③中外电路电子由a极流向b极 | |
| D. | 装置④的阳极反应为:2H++2e-=H2↑ |
20.NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 标准状况下,11.2 L乙醇所含分子数为0.5NA | |
| B. | 40 g氢氧化钠含有氧原子数为NA | |
| C. | 1mol任何纯净物都含有6.02×1023个原子 | |
| D. | 标准状况下,22.4 L氢气含有NA个氢原子 |
19.某无色溶液中含Na+、I-、NO3-、Cl-,加入下列哪种溶液不会使其变色( )
| A. | 酸化的淀粉溶液 | B. | 硫酸钠溶液 | C. | H2O2溶液 | D. | 氯水 |
18.25°C时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | c(H+)=1×10-13mol/L的溶液中:K+、Na+、NO3-、CH3COO- | |
| C. | 0.1mol•L-1NH4HCO3溶液:Na+、Fe3+、NO3-、Cl- | |
| D. | 0.1mol•L-1FeCl3溶液:Fe2+、NH4+、SCN-、SO42- |
16.类比推理是化学中常用的思维方法.下列推理正确的是( )
| A. | Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3 | |
| B. | SiH4的沸点高于CH4,推测H2S的沸点高于H2O | |
| C. | CO2是直线型分子,推测CS2也是直线型分子 | |
| D. | NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr |
15.下列物质按强电解质、弱电解质、酸性氧化物、碱性氧化物的组合中,正确的是( )
| 强电解质 | 弱电解质 | 酸性氧化物 | 碱性氧化物 | |
| A | H2SO4 | CH3COOH | NO2 | Na2O |
| B | BaSO4 | HClO | Mn2O7 | CaO |
| C | NaCl | 氨水 | SO2 | MnO2 |
| D | HI | HF | CO2 | Fe3O4 |
| A. | A | B. | B | C. | C | D. | D |
14.结合如图判断,下列叙述正确的是( )
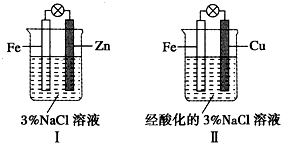

| A. | Ⅰ是验证牺牲阳极的阴极保护法的实验装置 | |
| B. | Ⅰ和Ⅱ中负极反应式均是:Fe-2e-=Fe2+ | |
| C. | Ⅰ和Ⅱ中正极反应式均是:2H++2e-=H2 | |
| D. | Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀 |
12.在标准状况下,1L N2中含m个氮分子,则阿伏加德罗常数可表示为( )
0 159337 159345 159351 159355 159361 159363 159367 159373 159375 159381 159387 159391 159393 159397 159403 159405 159411 159415 159417 159421 159423 159427 159429 159431 159432 159433 159435 159436 159437 159439 159441 159445 159447 159451 159453 159457 159463 159465 159471 159475 159477 159481 159487 159493 159495 159501 159505 159507 159513 159517 159523 159531 203614
| A. | $\frac{1}{28}$m/mol | B. | $\frac{1}{22.4}$m/mol | C. | 22.4m/mol | D. | 22.4 m/mol |
 “探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过.
“探险队员”--盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过.