1.在一个恒容绝热的容器内发生反应:mA(g)+nB(g)?pC(s)+qQ(g)当m、n、p、q为任意数时,达到平衡的标志是:( )
①体系的气体密度不再改变 ②体系的温度不再改变 ③生成物C的浓度不再改变
④气体的总质量不再改变 ⑤反应速率n v(A)=m v(B)
⑥单位时间内m mol A断键反应,同时q mol Q也断键反应.
①体系的气体密度不再改变 ②体系的温度不再改变 ③生成物C的浓度不再改变
④气体的总质量不再改变 ⑤反应速率n v(A)=m v(B)
⑥单位时间内m mol A断键反应,同时q mol Q也断键反应.
| A. | ①②④⑤ | B. | ②③④⑥ | C. | ①③④⑤ | D. | ①②④⑥ |
20.下列叙述不正确的是( )
| A. | 金属腐蚀的本质是金属原子失去电子而被氧化 | |
| B. | 钢铁吸氧腐蚀的正极反应是:O2+4e-+2H2O═4OH- | |
| C. | 将地下钢管与直流电源的正极相连,用来保护钢管 | |
| D. | 氢氧燃料电池中,氢气在负极发生氧化反应 |
19.某溶液中存在大量的OH-、CO32-、Cl-,该溶液中还可能大量存在的离子是( )
| A. | H+ | B. | NO3- | C. | Ag+ | D. | Ba2+ |
18.下列过程属于化学变化的是( )
| A. | 萃取分液 | B. | 石油的分馏 | C. | 蒸发结晶 | D. | 钢铁腐蚀 |
17.在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+和H2O,下列叙述正确的是( )
| A. | 为防止Fe2+水解,Fe(NO3)2溶液需要加酸酸化 | |
| B. | 该反应中氧化剂与还原剂物质的量之比为8:1 | |
| C. | 若有1molNO3-发生氧化反应,则转移电子5mol | |
| D. | 该反应中Fe2+是还原剂,NH4+是还原产物 |
16.下列说法正确的是( )
| A. | 氢氧燃料电池工作时,1mol H2在正极上失去2mol电子 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的CO32-的数目小于6.02×1022个 | |
| C. | 常温常压下,22.4LCl2中含有的分子数为6.02×1023个 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱 |
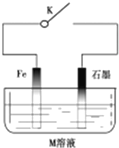
12.下列有关金属腐蚀与保护的说法正确的是( )
0 159333 159341 159347 159351 159357 159359 159363 159369 159371 159377 159383 159387 159389 159393 159399 159401 159407 159411 159413 159417 159419 159423 159425 159427 159428 159429 159431 159432 159433 159435 159437 159441 159443 159447 159449 159453 159459 159461 159467 159471 159473 159477 159483 159489 159491 159497 159501 159503 159509 159513 159519 159527 203614

| A. | 常温下,断开K时,若M溶液为浓硫酸,则铁发生化学腐蚀 | |
| B. | 关闭K,若M为氯化钠,则铁极的电极反应式为O2+4e-+2H2O=4OH- | |
| C. | 关闭K,若M为硫酸铵,则石墨极的电极反应式为2H++2e-=H2↑ | |
| D. | 关闭K,若M溶液为海水,石墨换成铜或银,则叫外加电流的阴极保护法 |
 如图所示进行实验:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.已知集气瓶的容积为150mL.氧气的密度为1.4g/L,为了节约药品.理论上所取硫的质量不能超过多少克?(要写过程,计算结果保留两位小数)
如图所示进行实验:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.已知集气瓶的容积为150mL.氧气的密度为1.4g/L,为了节约药品.理论上所取硫的质量不能超过多少克?(要写过程,计算结果保留两位小数)