20.实验室配制浓度为2.0mol•L-1 NaOH溶液100mL,下面有关操作及说法正确的是( )
| A. | 配制操作为:称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| B. | 称量 NaOH固体时,应在托盘天平两盘上各放一张大小相同的纸片 | |
| C. | 若所用NaOH固体中有少量Na2O杂质,则造成所配溶液浓度偏高 | |
| D. | 若用10 mol•L-1NaOH溶液来配制,用量筒量取20 mL NaOH浓溶液倒入烧杯后,应该用同一量筒取一定量蒸馏水倒入烧杯中 |
19.一块已被部分氧化为Na2O的钠块10.8g,将其投入一定量水中,最终得到含16g溶质的NaOH溶液,则原固体中氧化钠的质量是( )
| A. | 8.5 g | B. | 10.8 g | C. | 6.2 g | D. | 4.6 g |
18.在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g)△H未知,如图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )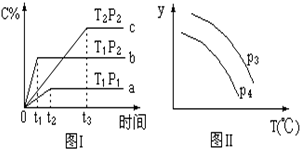

| A. | P3<P4,y轴表示A的转化率 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
17.NA表示阿佛加德罗常数的值,下列说法中正确的是( )
| A. | 7.8g Na2S和7.8g Na2O2中含有的阴离子数均为0.1NA | |
| B. | 0.1mol•L-1的NaHSO4溶液中含有阳离子物质的量为0.2mol | |
| C. | 常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L | |
| D. | 1.8g ${\;}_{8}^{18}$O2分子与1.6g ${\;}_{8}^{16}$O2分子中含有的中子数均为0.8NA |
16.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,11.2 L水中含有分子的数目为0.5NA | |
| B. | 100 mL 0.1 mol•L-1 Na2SO4溶液中,粒子总数是0.03NA | |
| C. | 标准状况下,33.6 LHF中含有氟原子的数目为1.5NA | |
| D. | 常温常压下,7.0 gC2H4与C3H6的混合物中含有氢原子的数目为NA |
14.下列说法正确的是( )
| A. | Fe在一定条件下与水反应生成H2和Fe(OH)3 | |
| B. | Fe3O4溶于盐酸后加入几滴KSCN溶液,溶液不显血红色 | |
| C. | FeCl2溶液蒸干后得到的是Fe(OH)3固体 | |
| D. | 将FeCl3饱和溶液滴入NaOH溶液中可制备Fe(OH)3胶体 |
11.“温室效应”是全球关注的环境问题之一.CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径.将CO2转化成有机物可有效实现碳循环.CO2转化成有机物的例子很多,如:
①6CO2+6H2O$\stackrel{光合作用}{→}$C6H12O6+6O2
②CO2+3H2$→_{△}^{催化剂}$CH3OH+H2O
③CO2+CH4$→_{△}^{催化剂}$CH3COOH
④2CO2+6H2$→_{△}^{催化剂}$CH2═CH2+4H2O
关于以上反应的说法,不正确的是( )
0 159305 159313 159319 159323 159329 159331 159335 159341 159343 159349 159355 159359 159361 159365 159371 159373 159379 159383 159385 159389 159391 159395 159397 159399 159400 159401 159403 159404 159405 159407 159409 159413 159415 159419 159421 159425 159431 159433 159439 159443 159445 159449 159455 159461 159463 159469 159473 159475 159481 159485 159491 159499 203614
①6CO2+6H2O$\stackrel{光合作用}{→}$C6H12O6+6O2
②CO2+3H2$→_{△}^{催化剂}$CH3OH+H2O
③CO2+CH4$→_{△}^{催化剂}$CH3COOH
④2CO2+6H2$→_{△}^{催化剂}$CH2═CH2+4H2O
关于以上反应的说法,不正确的是( )
| A. | 反应①是最节能的,同时原子利用率最高 | |
| B. | 反应①是最节能的,反应③的原子利用率最高 | |
| C. | 在反应②中,CO2作为氧化剂 | |
| D. | 反应④得到的产物可以作为生产塑料的原料 |
 .
.