20.氰(CN)2与氯气的性质相似,下表所示是氰与氯气的部分性质.( )
| 物质 | 熔点/℃ | 沸点/℃ | 水溶性 |
| (CN)2 | -34 | -21.2 | 可溶 |
| Cl2 | -101 | -34 | 可溶 |
| A. | 二者均为非金属单质 | |
| B. | 标况下,氰的体积大于氯气的体积 | |
| C. | 同温同压下,相同质量的氰和氯气,前者含有的原子多 | |
| D. | 标况下,氰与氯气的密度之比为71:52 |
17.在NaOH溶液中加入盐酸,至恰好完全反应,反应的微观示意图见如图.下列有关认识错误的是( )


| A. | 反应结束时溶液的pH=7 | |
| B. | 反应后溶液中存在的粒子只有Na+和Cl- | |
| C. | 该反应的实质是H+和OH-结合生成水 | |
| D. | 反应前后所有元素的化合价均无变化 |
16.硬铝的组成金属有铝、镁、铜、锰.已知:锰丝放入稀硫酸中,有气泡产生;锰丝放入硫酸铝溶液中,表面没有金属析出.下列有关金属的活动性强弱判断错误的是( )
| A. | Mn>Cu | B. | Al>Mn | C. | Mg>Al | D. | Mn>Mg |
15.下列应用化学科学对物质进行研究的基本方法或所得的结论,错误的是( )
| A. | 氢气和甲烷的密度都比空气的小,所以都可用向下排气法收集 | |
| B. | 配制溶质质量分数一定的溶液时,所用的烧杯必须是干燥的 | |
| C. | 蜡烛燃烧后质量变小,说明质量守恒定律不是普遍规律 | |
| D. | 通过测定两种稀盐酸的pH,可以比较它们的酸性强弱 |
13.已知:
①N2(g)+O2(g)=2NO(g)△H1=+180kJ•mol-1
②N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
0 159297 159305 159311 159315 159321 159323 159327 159333 159335 159341 159347 159351 159353 159357 159363 159365 159371 159375 159377 159381 159383 159387 159389 159391 159392 159393 159395 159396 159397 159399 159401 159405 159407 159411 159413 159417 159423 159425 159431 159435 159437 159441 159447 159453 159455 159461 159465 159467 159473 159477 159483 159491 203614
①N2(g)+O2(g)=2NO(g)△H1=+180kJ•mol-1
②N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)=2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
| A. | 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180 kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1molN2和3molH2,反应后放出的热量为Q1kJ,则Q1=92.4 | |
| D. | 氨的催化氧化反应为4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-906 kJ•mol-1 |
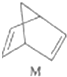 $?_{暗处}^{光照}$
$?_{暗处}^{光照}$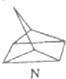 △H═88.6kJ•mol-1
△H═88.6kJ•mol-1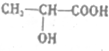 .
. .
. .
.