9.在200mL某硫酸盐溶液中含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为( )
| A. | 1 mol•L-1 | B. | 2.5 mol•L-1 | C. | 5 mol•L-1 | D. | 2 mol•L-1 |
8.下列离子方程式中不正确的是( )
| A. | 氢氧化钡溶液与硫酸混合:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 铁粉与硝酸银溶液反应:Fe+2Ag+═Fe2++2Ag | |
| C. | 氯化铝溶液与过量的氨水反应:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
7.下列实验操作先后顺序正确的是( )
| A. | 先装好药品,再检查装置的气密性 | |
| B. | 先用双手握紧试管,再将导管插入水中检查装置气密性 | |
| C. | 结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管 | |
| D. | 稀释硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
5.CoCl2•6H2O常用作多彩水泥的添加剂,以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种工艺如下:
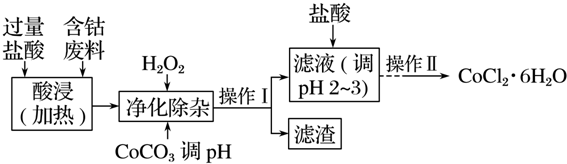
已知:
(1)净化除杂质时,加入H2O2发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.

已知:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
(2)加入CoCO3调pH为5.2~7.6,则操作Ⅰ获得的滤渣成分为Fe(OH)3、Al(OH)3.
(3)加盐酸调整pH为2~3的目的为抑制CoCl2水解.
(4)操作Ⅱ过程为蒸发浓缩、冷却结晶(填操作名称)、过滤、洗涤、干燥.其中洗涤的操作为在过滤器中加入蒸馏水使水没过晶体,静置,使其自然流下,重复2-3次.
4.有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;简单离子半径:B离子小于C离子(填“大于”或“小于”).
(3)D原子的外围电子排布式为3s23p5.
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应水化物反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,与C的最高价氧化物对应水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式1s22s22p63s1.
(2)B元素在周期表中的位置第3周期第ⅢA族;简单离子半径:B离子小于C离子(填“大于”或“小于”).
(3)D原子的外围电子排布式为3s23p5.
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应水化物反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,与C的最高价氧化物对应水化物反应的离子方程式为Al(OH)3+3H+=Al3++3H2O.
3.下表为元素周期表中第四周期的部分元素(从左到右按原子序数递增排列),根据要求回答下列问题:
(1)在以上元素的基态原子的电子排布中4s轨道上只有1个电子的元素有钾、铬、铜(填元素名称).
(2)写出Cr3+的电子排布式[Ar]3d3 ;元素周期表分为五个区域,Ga属于p区元素.
(3)Fe3+的化学性质比Fe2+稳定,其原因是Fe3+的3d轨道为半充满状态.
(4)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有5种.
(5)试比较:第一电离能I1(K)<I1(Ca)(填“>”、“<”或“=”).
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
(2)写出Cr3+的电子排布式[Ar]3d3 ;元素周期表分为五个区域,Ga属于p区元素.
(3)Fe3+的化学性质比Fe2+稳定,其原因是Fe3+的3d轨道为半充满状态.
(4)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有5种.
(5)试比较:第一电离能I1(K)<I1(Ca)(填“>”、“<”或“=”).
2.下列离子组在指定溶液中能大量共存的是( )
| A. | 常温下,c(H+)/c(OH一)=1×10-12的溶液:K+、AlO2-、SiO32-、Na+ | |
| B. | 加入KSCN显红色的溶液:K+、NH4+、Cl-、I- | |
| C. | 加入石蕊显蓝色的溶液:Cu2+、Al3+、NO3-、SO42- | |
| D. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- |
1.将pH=1的稀硫酸慢慢加入一定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度约为( )
0 159290 159298 159304 159308 159314 159316 159320 159326 159328 159334 159340 159344 159346 159350 159356 159358 159364 159368 159370 159374 159376 159380 159382 159384 159385 159386 159388 159389 159390 159392 159394 159398 159400 159404 159406 159410 159416 159418 159424 159428 159430 159434 159440 159446 159448 159454 159458 159460 159466 159470 159476 159484 203614
| A. | 0.22 mol/L | B. | 0.11 mol/L | C. | 0.022 mol/L | D. | 0.011 mol/L |
 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、乙酸,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、乙酸,D中放有饱和碳酸钠溶液. .
.