12.已知:某密闭容器中,12gA加热完全分解产生B和C,其中B的质量为2g,同时C又能部分分解产生0.1gD和7.9gE,则最终该密闭容器中B和C的质量比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:4 | D. | 1:5 |
11.每l00g草鱼中所含主要营养成分的平均质量为
则该草鱼能提供人类生命活动必需的营养素有( )
| 成分 | 糖类 | 蛋白质 | 油脂 | 水 | 维生素 | 钙 | 铁 | 锌 |
| 质量/g | 0 | 16.6 | 5.2 | 78.2 | 0.00004 | 0.038 | 0.0008 | 0.0009 |
| A. | 六大类 | B. | 五大类 | C. | 四大娄 | D. | 三大类 |
9.在PH=1的溶液中,下列各组离子一定能存在的是( )
| A. | Na+、NO3-、Al3+、K+ | B. | Na+、ClO3-、ClO-、ClO4- | ||
| C. | K+、Cr2O72-、I-、Na+ | D. | Na+、SO32-、SO42-、NH4+ |
8.下列反应的可能为4Al3++13OH-=AlO2-+3Al(OH)3↓+2H2O的是( )
| A. | 在氯化铝溶液中滴加氨水 | B. | 在偏铝酸钠溶液中通入CO2 | ||
| C. | 在氯化铝溶液中滴加氢氧化钠溶液 | D. | 在硫酸铝溶液中滴加偏铝酸钠溶液 |
7.下列有关说法正确的是( )
| A. | 分离碘单质和四氯化碳的混合物需要烧杯、玻璃棒和漏斗 | |
| B. | 用湿润的pH试纸测定溶液的pH一定会产生误差 | |
| C. | 实验室可以向浓硫酸中滴加浓盐酸制取少量氯化氢 | |
| D. | 用浓氨水可以除去试管内壁银镜 |
5.下列离子方程式中,只能表示一个化学反应的是( )
①Fe+Cu2+═Fe2++Cu
②Al3++3NH3•H2O═Al(OH)3↓+3NH4+
③Cl2+H2O?H++Cl-+HClO
④CaCO3+2H+═Ca2++CO2↑+H2O
⑤Ag++Cl-═AgCl↓
①Fe+Cu2+═Fe2++Cu
②Al3++3NH3•H2O═Al(OH)3↓+3NH4+
③Cl2+H2O?H++Cl-+HClO
④CaCO3+2H+═Ca2++CO2↑+H2O
⑤Ag++Cl-═AgCl↓
| A. | ③⑤ | B. | ②③ | C. | 只有③ | D. | ①④ |
3.连二亚硫酸钠(Na2S2O4)是印刷工业中重要的还原剂.某小组进行如下实验:
已知:
①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.
②、4HCl+2Na2S2O4=4NaCl+S↓+3SO2↑+2H2O
I.制备
75℃时,将甲酸钠和纯碱加入乙醇水溶液溶解后,再加入装置 C 中,然后通入 SO2 进 行反应,其反应方程式为:2HCOONa+Na2CO3+4SO2=2Na2S2O4+3CO2+H2O.
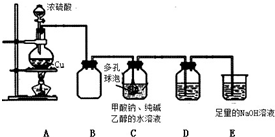
分析并回答下列问题:
(1)A 中反应的化学方程式为Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;冷却至 40~50℃,过 滤,用乙醇洗涤,干燥制得 Na2S2O4.
(2)C 中多孔球泡的作用是 增大接触面积,促进SO2的吸收
(3)装置 D 盛放品红溶液,作用是检验装置 C 中 SO2 的吸收效率,若在吸收过程中 D
中颜色逐渐褪去,此时应该采取的措施是撤去A中酒精灯,减缓SO2的生成速率
II.【Na2S2O4 的性质】
取纯净的 Na2S2O4 晶体,配成溶液,进行下列性质探究实验,完成表的空格
(供选择的试剂:淀粉-KI 溶液、紫色石蕊试液、稀硝酸、BaCl2 溶液)
III.【测定 Na2S2O4的纯度】
取 8.00g 制备的晶体溶解后,加入足量稀硫酸,充分反应后,过滤、洗涤、干燥.得固 体 0.64g.则 Na2S2O4的纯度为87%[已知:M(Na2S2O4)=174.0].
0 159272 159280 159286 159290 159296 159298 159302 159308 159310 159316 159322 159326 159328 159332 159338 159340 159346 159350 159352 159356 159358 159362 159364 159366 159367 159368 159370 159371 159372 159374 159376 159380 159382 159386 159388 159392 159398 159400 159406 159410 159412 159416 159422 159428 159430 159436 159440 159442 159448 159452 159458 159466 203614
已知:
①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.
②、4HCl+2Na2S2O4=4NaCl+S↓+3SO2↑+2H2O
I.制备
75℃时,将甲酸钠和纯碱加入乙醇水溶液溶解后,再加入装置 C 中,然后通入 SO2 进 行反应,其反应方程式为:2HCOONa+Na2CO3+4SO2=2Na2S2O4+3CO2+H2O.

分析并回答下列问题:
(1)A 中反应的化学方程式为Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;冷却至 40~50℃,过 滤,用乙醇洗涤,干燥制得 Na2S2O4.
(2)C 中多孔球泡的作用是 增大接触面积,促进SO2的吸收
(3)装置 D 盛放品红溶液,作用是检验装置 C 中 SO2 的吸收效率,若在吸收过程中 D
中颜色逐渐褪去,此时应该采取的措施是撤去A中酒精灯,减缓SO2的生成速率
II.【Na2S2O4 的性质】
取纯净的 Na2S2O4 晶体,配成溶液,进行下列性质探究实验,完成表的空格
(供选择的试剂:淀粉-KI 溶液、紫色石蕊试液、稀硝酸、BaCl2 溶液)
| 假 设 | 操作 | 现 象 | 原理 |
| Na2S2O4 为强 碱弱酸盐,其溶 液为碱性. | 取少量溶液于试管中,滴加 紫色石蕊试液 | 溶液变 成蓝色 | S2O42-水解,使溶液成碱性 |
| Na2S2O4 中 S 为 +3 价,具有较强 的还原性. | 取少量溶液于试管中,滴加过量新制氯水,再 滴加 BaCl2 溶液 | 有白色沉淀生 成 | 该反应的离子方程式依次为: 4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+ Ba2++SO42-=BaSO4↓ |
取 8.00g 制备的晶体溶解后,加入足量稀硫酸,充分反应后,过滤、洗涤、干燥.得固 体 0.64g.则 Na2S2O4的纯度为87%[已知:M(Na2S2O4)=174.0].
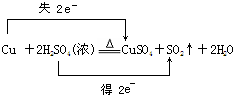 .
.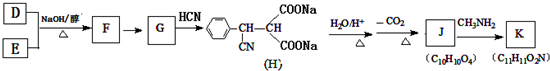
 ,则 D 的核磁共振氢谱有6种峰.F 中的无氧官能团为碳碳双键.
,则 D 的核磁共振氢谱有6种峰.F 中的无氧官能团为碳碳双键.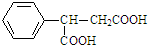 +CH3NH2$\stackrel{一定条件下}{→}$
+CH3NH2$\stackrel{一定条件下}{→}$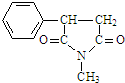 +2H2O.
+2H2O.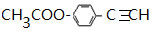 .
.