12.下列图①~④分别与相应的操作过程相对应,其中正确的是( )
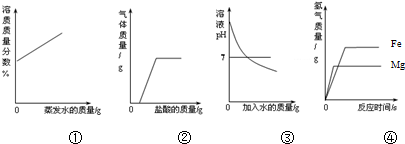

| A. | ①在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分 | |
| B. | ②向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸 | |
| C. | ③向氢氧化钠溶液中不断加水稀释 | |
| D. | ④相同质量的且过量的镁粉和铁粉,分别与质量和质量分数相同的稀盐酸反应 |
11.煤炭含硫量约为4%~6%,燃烧时产生SO2 等大气污染物,为保护环境,下列措施中不能采取的是( )
| A. | 高烟囱排放 | B. | 用氨水吸收后排放 | ||
| C. | 用烧碱吸收后排放 | D. | 用活性炭吸收后排放 |
10.环境污染已成为人类社会面临的重大威胁.下列名词与环境污染无关的是…( )
①温室效应; ②赤潮; ③酸雨; ④光化学污染;
⑤臭氧空洞; ⑥水俣病; ⑦潮汐; ⑧大脖子病.
①温室效应; ②赤潮; ③酸雨; ④光化学污染;
⑤臭氧空洞; ⑥水俣病; ⑦潮汐; ⑧大脖子病.
| A. | ②⑧ | B. | ⑦⑧ | C. | ⑥⑦⑧ | D. | ②⑤⑦ |
9.配制500mL0.1mol/L的NaOH溶液,下列操作会使溶液的物质的量浓度偏大的是( )
| A. | 定容时,仰视刻度线 | B. | 称量用了生锈的砝码 | ||
| C. | 未洗涤溶解NaOH的烧杯 | D. | 容量瓶未经过干燥即用来配制溶液 |
8.《中华人民共和国大气污染防治法》于2016年1月1日起实施.为保护和改善大气环境,下列做法不应该提倡的是( )
| A. | 用CO2合成聚碳酸酯等可降解塑料,减少白色污染 | |
| B. | 研究采煤、采油新技术,尽量提高其产量以满足工业生产快速发展的需求 | |
| C. | 大力推广农作物的生物防治技术,以减少农药的使用 | |
| D. | 研发光电转换材料,充分利用太阳能 |
7.下列说法正确的是( )
| A. | 用KSCN溶于检验Fe2(SO4)3溶液中是否含有FeSO4 | |
| B. | 由同种元素组成的物质一定是纯净物 | |
| C. | 将钢闸门与电源正极相连,可防止其在海水中被腐蚀 | |
| D. | 浊液、胶体、溶液三种分散系的本质区别是分散质微粒直径的大小不同 |
6.化学与生活息息相关,下列说法不正确的是( )
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 用食醋可除去热水壶内壁的水垢 | |
| C. | 烹鱼时加适量醋和酒可以增加香味 | |
| D. | 医用酒精消毒是利用其氧化性使蛋白质变性 |
5.如图,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为( )


| A. | ①②③④⑤ | B. | ④③②①⑤ | C. | ④③①②⑤ | D. | ④②③①⑤ |
3.下列说法错误的是( )
0 159266 159274 159280 159284 159290 159292 159296 159302 159304 159310 159316 159320 159322 159326 159332 159334 159340 159344 159346 159350 159352 159356 159358 159360 159361 159362 159364 159365 159366 159368 159370 159374 159376 159380 159382 159386 159392 159394 159400 159404 159406 159410 159416 159422 159424 159430 159434 159436 159442 159446 159452 159460 203614
| A. | 将煤气化后再作为能源,可减少PM2.5引起的危害 | |
| B. | 农作物秸秆处理起来麻烦,利用价值低,适于就地露天焚烧 | |
| C. | 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理 | |
| D. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
