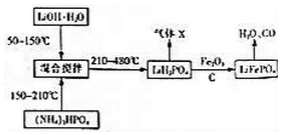
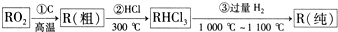8.从理论上讲,一切自发的氧化还原反应均可设计成原电池,下列不正确的是( )
| A. | 非自发的氧化还原反应不可以设计成原电池 | |
| B. | 将反应 3Cu+8HNO3═3Cu(NO3)2+2NO+4H2O 设计成原电池,其正极反应为:2NO3-+6e-+8H+═2NO+4H2O | |
| C. | 铅蓄电池工作时,正极、负极质量均增加 | |
| D. | 氢氧燃料电池耗H20.1mol时,电路中流经的电子数为0.1NA |
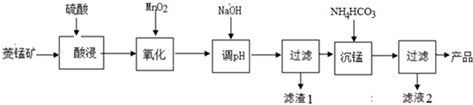
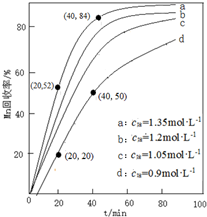
6.碳酸镍可用于电镀、陶瓷器着色等.镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS(含有Fe、Cu、Ca、Mg、Zn等元素杂质),从镍矿渣出发制备碳酸镍的流程如下:
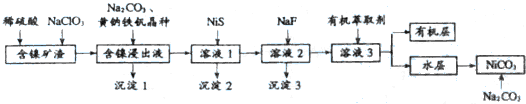
已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:
(Ⅱ)溶度积常数:
(1)镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,写出浸取时反应的离子方程式3NiS+4ClO3-=3Ni2++3SO42-+4Cl-或3NiS+ClO3-+6H+=3Ni2++3S+Cl-+3H2O.
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁.写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:Na++3Fe3++2SO42-+3H2O+3CO32-=NaFe3(SO4)2(OH)6↓+3CO2↑;
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+═CuS+Ni2+,该反应的平衡常数是8.43×104;
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是Mg2+.
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②过滤,并用蒸馏水洗涤沉淀2-3次直至流出液用pH试纸检验呈中性;
③向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解;
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干.
确定步骤①中Na2CO3溶液足量,碳酸镍己完全沉淀的简单方法是:上层清液呈无色(或静置后向上层液中再加入Na2CO3溶液后没有沉淀生成);
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】.

已知:(Ⅰ)含镍浸出液的成分及离子沉淀的pH:
| 元素 | Na2+ | Fe3+ | Cu2+ | Ca2+ | Mg2+ | Zn2- |
| 浓度/g•L-1 | 5.25 | 0.47 | 0.30 | 0.40 | 0.18 | 0.81 |
| 开始沉淀PH | 6.4 | 2.2 | 4.7 | / | 9.6 | 6.5 |
| 完全沉淀PH | 8.4 | 3.5 | 6.7 | / | 11.6 | 8.5 |
| 难溶物 | NiS | CuS | ZnS | |
| 溶度积常数 | 1.07×10-21 | 1.27×10-26 | 2.93×10-25 | |
| 难溶物 | CaF2 | MgF2 | ZnF2 | NiF2 |
| 溶度积常数 | 1.46×10-10 | 7.42×10-11 | 3.04×10-2 | 微溶 |
(2)黄钠铁钒[NaFe3(SO4)2(OH)6]具有沉淀颗粒大、沉淀速度快,容易过滤等特点,常用于除铁.写出流程中第一次加入 Na2CO3溶液时反应的离子方程式:Na++3Fe3++2SO42-+3H2O+3CO32-=NaFe3(SO4)2(OH)6↓+3CO2↑;
(3)NiS的作用是除去溶液中的Cu2+,原理是NiS+Cu2+═CuS+Ni2+,该反应的平衡常数是8.43×104;
(4)滤液2中加入NaF的作用是除去溶液中的Ca2+、Mg2+,则加入NaF先沉淀的离子是Mg2+.
(5)NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由NiCO3为原料获得,结合上述流程,制备NiSO4•6H2O的操作步骤如下:
①向被有机萃取剂萃取后所得的水层中加入足量Na2CO3溶液(流程中第二次加Na2CO3溶液),搅拌,得NiCO3沉淀:
②过滤,并用蒸馏水洗涤沉淀2-3次直至流出液用pH试纸检验呈中性;
③向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解;
④蒸发、冷却结晶并从溶液中分离出晶体;
⑤用少量乙醇洗涤并晾干.
确定步骤①中Na2CO3溶液足量,碳酸镍己完全沉淀的简单方法是:上层清液呈无色(或静置后向上层液中再加入Na2CO3溶液后没有沉淀生成);
补充完整上述步骤②和③【可提供的试剂有6mol/L的H2SO4溶液,蒸馏水、pH试纸】.
5.实验室用乙酸和正丁醇制备乙酸正丁酯,有关物质的物理性质如表,请回答有关问题
Ⅰ.乙酸正丁酯粗产品的制备
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)写出乙酸正丁酯制备的化学方程式:CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.本实验过程中可能产生多种有机副产物,写出其中一种的结构简式:CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3.
(2)在乙酸乙酯的制备过程中采用了“边反应边蒸馏”的方式收集乙酸乙酯,乙酸正丁酯的制备过程中能否采用“边反应边蒸馏”的方式?为什么?不可以.因为乙酸正丁酯的沸点比乙酸和正丁醇都高
Ⅱ.乙酸正丁酯精产品的制备
(1)将乙酸正丁酯粗产品用如下操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用15%碳酸钠溶液洗涤,正确的操作步骤是C(填字母).
AA.①②③④B.③①④②
C.①④①③②D.④①③②③
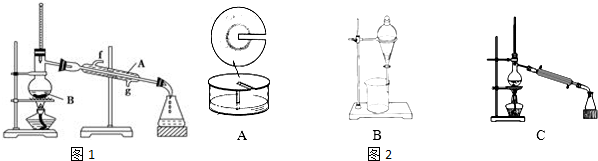
(2)将酯层采用如图1所示装置蒸馏.
①写出图1中仪器A的名称冷凝管,冷却水从g口进入(填字母).
②蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃左右.
Ⅲ.计算产率
(1)测量分水器内由乙酸与正丁醇反应生成水的体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率为79.4%.实验中为了提高乙酸正丁酯的产率,采取的措施是BC
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(2)正丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列C(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液.
0 159262 159270 159276 159280 159286 159288 159292 159298 159300 159306 159312 159316 159318 159322 159328 159330 159336 159340 159342 159346 159348 159352 159354 159356 159357 159358 159360 159361 159362 159364 159366 159370 159372 159376 159378 159382 159388 159390 159396 159400 159402 159406 159412 159418 159420 159426 159430 159432 159438 159442 159448 159456 203614
| 化合物 | 密度/g•cm-3 | 沸点/℃ | 溶解性 |
| 正丁醇 | 0.810 | 118.0 | 可溶 |
| 冰醋酸 | 1.049 | 118.1 | 互溶 |
| 乙酸正丁酯 | 0.882 | 126.1 | 微溶 |
| 乙醇 | 0.79 | 78.5 | 互溶 |
| 乙酸乙酯 | 0.88 | 77.06 | 可溶 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)写出乙酸正丁酯制备的化学方程式:CH3COOH+CH3CH2CH2CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O.本实验过程中可能产生多种有机副产物,写出其中一种的结构简式:CH2═CHCH2CH3或CH3CH2CH2CH2OCH2CH2CH2CH3.
(2)在乙酸乙酯的制备过程中采用了“边反应边蒸馏”的方式收集乙酸乙酯,乙酸正丁酯的制备过程中能否采用“边反应边蒸馏”的方式?为什么?不可以.因为乙酸正丁酯的沸点比乙酸和正丁醇都高
Ⅱ.乙酸正丁酯精产品的制备
(1)将乙酸正丁酯粗产品用如下操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用15%碳酸钠溶液洗涤,正确的操作步骤是C(填字母).
AA.①②③④B.③①④②
C.①④①③②D.④①③②③
(2)将酯层采用如图1所示装置蒸馏.
①写出图1中仪器A的名称冷凝管,冷却水从g口进入(填字母).
②蒸馏收集乙酸正丁酯产品时,应将温度控制在126.1℃左右.
Ⅲ.计算产率
(1)测量分水器内由乙酸与正丁醇反应生成水的体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率为79.4%.实验中为了提高乙酸正丁酯的产率,采取的措施是BC
A.使用催化剂 B.加过量乙酸 C.不断移去产物 D.缩短反应时间
(2)正丁醇若含有乙醇,有同学认为制得的乙酸丁酯中含有乙酸乙酯.为了证实该观点,可尝试选用下列C(填序号)装置来做实验,请简述与实验结论有关的实验过程和现象将制得的乙酸丁酯进行蒸馏,看能否得到78℃左右的馏分,且该馏分不溶于饱和碳酸钠溶液.

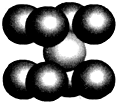 已知A、B、R、D都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素.
已知A、B、R、D都是周期表中前四周期的元素,它们的原子序数依次增大.其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素.