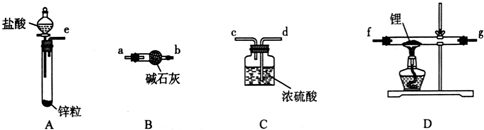
1. 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
 常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )
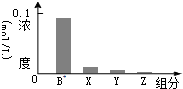
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是 ( )| A. | HA为强酸 | B. | 该混合溶液中:c(A-)+c(Y)=c(Na+) | ||
| C. | 图中X表示HA,Y表示H+,Z表示OH- | D. | 该混合液pH=7 |
5.足量的铝粉投入20mLNaOH溶液中,充分反应后放出标准状况下H26.72L,则NaOH溶液的物质的量浓度为( )
| A. | 15mol•L-1 | B. | 10mol•L-1 | C. | 5mol•L-1 | D. | 1mol•L-1 |
3.金属氢化物是常用的供氢剂,已知2240mL(标准状况)氢气与足量的锂完全反应生成氢化锂(H2+2Li=2LiH),这些氢化锂与足量的水反应(LiH+H2O=LiOH+H2),产生的氢气构成氢氧碱性燃料电池,完全放电时电路通过0.32mol电子,则该氢氧燃料电池的能量转化率为( )
| A. | 60% | B. | 75% | C. | 80% | D. | 85% |
2.10mL 0.1mol/L KI与10mL 0.05mol/L AgNO3溶液混合制得AgI溶胶,用下述电解质使该溶胶聚沉,聚沉能力最大的是( )
| A. | NaCl | B. | KNO3 | C. | MgSO4 | D. | AlCl3 |
1.下列说法不正确的是( )
| A. | 物质所含元素化合价升高的反应是氧化反应 | |
| B. | 物质所含元素化合价降低的反应是还原反应 | |
| C. | 氧化剂本身被还原,具有氧化性;还原剂本身被氧化,具有还原性 | |
| D. | 氧化反应和还原反应不一定同时存在于一个反应中 |
20.在某无色透明酸性溶液中,能共存的离子组是( )
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、Al3+、S2-、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | K+、SO42-、HCO3-、Na+ |
18.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO,下列叙述正确的是( )
0 159261 159269 159275 159279 159285 159287 159291 159297 159299 159305 159311 159315 159317 159321 159327 159329 159335 159339 159341 159345 159347 159351 159353 159355 159356 159357 159359 159360 159361 159363 159365 159369 159371 159375 159377 159381 159387 159389 159395 159399 159401 159405 159411 159417 159419 159425 159429 159431 159437 159441 159447 159455 203614
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中每生成2 mol AlN,N2得到3 mol | |
| C. | 氮化铝中氮元素的化合价为-3 | |
| D. | 氮化铝晶体属于分子晶体,熔点和沸点较低 |