7.将amolH2和Cl2的混合气体点燃,充分反应后用足量的NaOH溶液吸收,消耗了bmolNaOH.
(1)填表
(2)以n(Cl2)为横坐标,n(NaCl)为纵坐标,作出生成的NaCl与消耗的Cl2的关系图.
(1)填表
| H2和Cl2的物质的量关系 | n(H2)=n(Cl2) | n(H2)>n(Cl2) | n(H2)<n(Cl2) |
| 生成NaCl的物质的量 | amol(或bmol) | bmol | amol |
6.100mL 2mol•L-l硫酸跟过量的锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A. | 硝酸钾 | B. | 醋酸钠 | C. | 硫酸氢钠 | D. | 硫酸铜 |
5.已知下面表格中的数据,
根据上述表格中的数据,推断下列反应为吸热反应的是( )
①2H2O(g)═2H2(g)+O2(g)②H2(g)+Cl2(g)═2HCl(g)③H2(g)+Br2(g)═2HBr(g)④2HI(g)═H2(g)+I2(g)
| 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 | 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 | 共价键 | 断开该键吸收的能量或生成该键放出的能量/kJ•mol-1 |
| H-H | 436 | H-Br | 366 | Cl-Cl | 243 |
| H-O | 463 | H-I | 298 | Br-Br | 193 |
| H-Cl | 432 | O=O | 496 | I-I | 151 |
①2H2O(g)═2H2(g)+O2(g)②H2(g)+Cl2(g)═2HCl(g)③H2(g)+Br2(g)═2HBr(g)④2HI(g)═H2(g)+I2(g)
| A. | ①④ | B. | ②③ | C. | 只有① | D. | 只有④ |
4.设NA代表阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,18gH218O所含质子数为10NA | |
| B. | 1 mol乙醇中含有极性键的数目为8NA | |
| C. | 1mol的-NH2与1molNH4+所含电子数均为10NA | |
| D. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
3.工业上由钛铁矿(主要成分是FeTiO3钛酸亚铁)制备TiCl4.流程如图所示: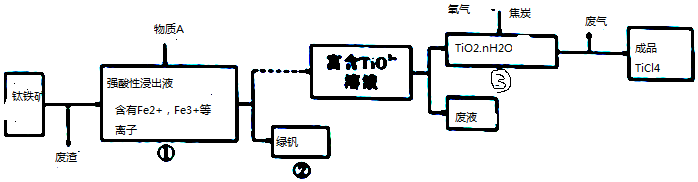
(1)FeTiO3中,Ti元素的化合价为+4.
(2)往①中加入的物质A是Fe.
(3)②中的绿矾带有棕黄色,原因可能是含有Fe3+;设计实验证明Fe3+杂质离子的存在取样,溶于水,向溶液中加入KSCN溶液,如果溶液变为血红色,证明含有Fe3+;
(4)写出③中TiO2和过量焦炭、氯气在高温下反应的化学方程式:TiO2+2C+Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.
(5)用金属Mg还原成品TiO4得到Mg、MgCl2和Ti的混合物,再真空蒸馏制备Ti. 依据下表,蒸馏温度略高于1412℃即可.
(6)依据绿色化学理念.该制备流程中存在明显的不足之处是三废没有处理.
(7)向含有Fe2+、Fe3+溶液加入适量KOH和油脂,在高速撞拌下得到磁流体材料KxFeO2.
①若x=l.请写出在酸性条件下KxFeO2溶液与足量KI溶液反应的离子方程式:8H++2FeO2-+2I-=2Fe2++I2+4H2O.
②磁流体材料KxFeO2在组成上可理解为aK2O•bFeO•cFe2O3,若x=1.3,则b:c=6:7.

(1)FeTiO3中,Ti元素的化合价为+4.
(2)往①中加入的物质A是Fe.
(3)②中的绿矾带有棕黄色,原因可能是含有Fe3+;设计实验证明Fe3+杂质离子的存在取样,溶于水,向溶液中加入KSCN溶液,如果溶液变为血红色,证明含有Fe3+;
(4)写出③中TiO2和过量焦炭、氯气在高温下反应的化学方程式:TiO2+2C+Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.
(5)用金属Mg还原成品TiO4得到Mg、MgCl2和Ti的混合物,再真空蒸馏制备Ti. 依据下表,蒸馏温度略高于1412℃即可.
| Mg | MgCl2 | Ti | |
| 熔点/℃ | 648.0 | 714 | 1667 |
| 沸点/℃ | 1090 | 1412 | 3287 |
(7)向含有Fe2+、Fe3+溶液加入适量KOH和油脂,在高速撞拌下得到磁流体材料KxFeO2.
①若x=l.请写出在酸性条件下KxFeO2溶液与足量KI溶液反应的离子方程式:8H++2FeO2-+2I-=2Fe2++I2+4H2O.
②磁流体材料KxFeO2在组成上可理解为aK2O•bFeO•cFe2O3,若x=1.3,则b:c=6:7.
20.化学键的键能是指气态基态原子间形成1mol 化学键时释放的最低能量.如:H(g)+I(g)-→H-I(g)+297kJ,即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297kJ的热量.化学反应的发生可以看成旧化学键的破坏和新化学键的形成.
表是一些键能数据(单位:kJ/mol):
阅读上述信息,回答下列问题:
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
表是一些键能数据(单位:kJ/mol):
| 键能 | 键能 | 键能 | |||||
| H-H | 436 | Cl-Cl | 243 | H-Cl | 432 | ||
| S-S | 255 | H-S | 339 | C-F | 427 | ||
| C-Cl | 330 | C-I | 218 | H-F | 568 | ||
| C-O | 351 | H-O | 463 |
(1)根据表中数据判断CCl4的稳定性小于(填“大于”或“小于”)CF4的稳定性.试预测C-Br键的键能范围:218 kJ/mol<C-Br键键能<330 kJ/mol.
(2)结合表中数据和热化学方程式H2(g)+Cl2(g)═2HCl(g)△H=-Q kJ/mol,则热化学方程式中Q的值为185.
(3)由表中数据能否得出这样的结论:
①半径越小的原子形成的共价键越牢固(即键能越大).不能(填“能”或“不能”).
②非金属性越强的原子形成的共价键越牢固.不能(填“能”或“不能”).从数据中找出一些规律,请写出一条:与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越强.
18.研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)已知石墨的标准燃烧热为y kJ•mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-(20x-y)kJ•mol-1.
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=$\frac{C(CH{\;}_{3}OH)C(H{\;}_{2}O)}{C(CO{\;}_{2})C{\;}^{3}(H{\;}_{2})}$.
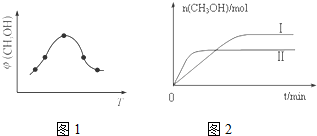
②取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇反应的△H<(填“>”“<”或“=”)0.
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”“<”或“=”).
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡.
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为0.4<n(c)≤1mol.
0 159257 159265 159271 159275 159281 159283 159287 159293 159295 159301 159307 159311 159313 159317 159323 159325 159331 159335 159337 159341 159343 159347 159349 159351 159352 159353 159355 159356 159357 159359 159361 159365 159367 159371 159373 159377 159383 159385 159391 159395 159397 159401 159407 159413 159415 159421 159425 159427 159433 159437 159443 159451 203614
(1)已知石墨的标准燃烧热为y kJ•mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量,则石墨与氧气反应生成CO的热化学方程式为C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-(20x-y)kJ•mol-1.

(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=$\frac{C(CH{\;}_{3}OH)C(H{\;}_{2}O)}{C(CO{\;}_{2})C{\;}^{3}(H{\;}_{2})}$.
②取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图1所示,则上述CO2转化为甲醇反应的△H<(填“>”“<”或“=”)0.
③在两种不同温度下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”“<”或“=”).
④一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2 3molH2 | a molCO2、b molH2、c molCH3OH(g)、c molH2O(g) (a、b、c均不等于0) |
 有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:
有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系: