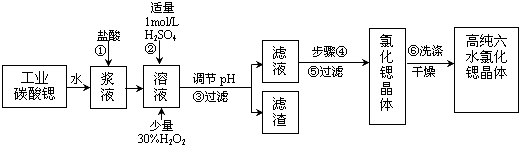
17.工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2•6H2O),其过程为:
已知:Ⅰ.有关氢氧化物沉淀的pH:
Ⅱ.SrCl2•6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
(1)操作①中碳酸锶与盐酸反应的离子方程式SrCO3+2H+=Sr2++CO2↑+H2O.
(2)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为E.
A.1.5 B.3.7 C.9.7
D氨水 E氢氧化锶粉末 F碳酸钠晶体
(3)操作②中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4(填化学式).
(5)工业上用热风吹干六水氯化锶,适宜的温度是A.
A.50~60℃B.80~100℃C.100℃以上
(6)步骤⑥宜选用的无机洗涤剂是饱和氯化锶溶液.

已知:Ⅰ.有关氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
(1)操作①中碳酸锶与盐酸反应的离子方程式SrCO3+2H+=Sr2++CO2↑+H2O.
(2)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为E.
A.1.5 B.3.7 C.9.7
D氨水 E氢氧化锶粉末 F碳酸钠晶体
(3)操作②中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4(填化学式).
(5)工业上用热风吹干六水氯化锶,适宜的温度是A.
A.50~60℃B.80~100℃C.100℃以上
(6)步骤⑥宜选用的无机洗涤剂是饱和氯化锶溶液.
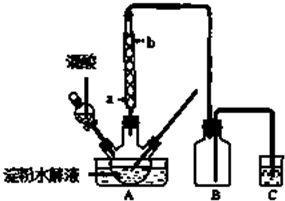
16.青蒿素是烃的含氧衍生物,为无色针状晶体.易溶于丙酮、氯仿和苯中,在水中几乎不溶,熔点为156-157℃.青蒿素是有效的抗疟药.从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为:
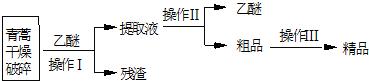
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作I的名称是过滤,操作II的名称是蒸馏.
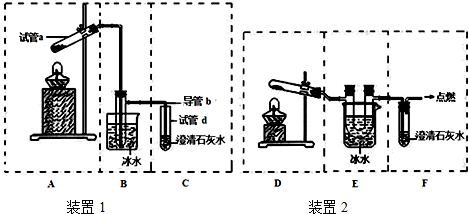
(3)用下列实验装置测定青蒿素的分子式,将28.2g青蒿素放在硬质玻璃管C中充分燃烧:
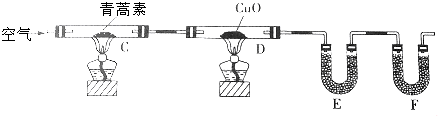
①装置E中盛放的物质是无水CaCl2或P2O5,装置F中盛放的物质是碱石灰.
②该实验装置可能产生误差,造成测定含氧量偏低,改进方法是除去装置左侧通入的空气中的CO2和水蒸气,在装置F后加一个防止空气中的CO2和水蒸气进入F的装置.
③已知青蒿素是烃的含氧衍生物,用合理改进后的装置进行实验,称得:
青蒿素的最简式是15H22O5.
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与C(填字母)具有相似的性质.
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素的浸取率.
(2)操作I的名称是过滤,操作II的名称是蒸馏.
(3)用下列实验装置测定青蒿素的分子式,将28.2g青蒿素放在硬质玻璃管C中充分燃烧:

①装置E中盛放的物质是无水CaCl2或P2O5,装置F中盛放的物质是碱石灰.
②该实验装置可能产生误差,造成测定含氧量偏低,改进方法是除去装置左侧通入的空气中的CO2和水蒸气,在装置F后加一个防止空气中的CO2和水蒸气进入F的装置.
③已知青蒿素是烃的含氧衍生物,用合理改进后的装置进行实验,称得:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与C(填字母)具有相似的性质.
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖.
14.根据热化学方程式S(l)+O2(g)═SO2(g)△H=-293.23kJ•mol-1分析,下列说法中正确的是( )
| A. | S(s)+O2(g)═SO2(g),反应放出的热量大于293.23 kJ•mol-1 | |
| B. | S(g)+O2(g)═SO2(g),反应放出的热量小于293.23 kJ•mol-1 | |
| C. | 1 mol SO2的键能总和大于1 mol硫和1 mol氧气的键能之和 | |
| D. | 1 mol SO2的键能总和小于1 mol硫和1 mol氧气的键能之和 |
12.碘酸钙[Ca(IO3)2]既能补碘又能补钙的新型食品和饲料添加剂.碘酸钙可通过下列途径合成.
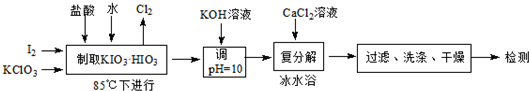
(1)若称取的I2质量为3.810g,为使I2充分氧化,则投料时KClO3的质量至少为3.675;同时生成的氯气体积为336mL(标准状况).
(2)用KOH溶液调节pH的目的是将KIO3•HIO3转变为KIO3.
(3)已知几种盐的溶解度(g/100g水)如下:
碘酸钙的物理性质
复分解时,采用冰水浴的目的是减小Ca(IO3)2在水中的溶解度,使其充分析出;此时所得产品的化学式为Ca(IO3)2•6H2O.
(4)准确称取产品0.6000g于烧标中,加1:1高氯酸20mL,微热溶解后,冷却,配成250.00mL溶液.移取上述溶液50.00mL置于250mL碘量瓶中,加入1:1高氯酸2mL、3gKI(足量)(发生:IO3-+5I-+6H+═3I2+3H2O),盖上瓶盖,暗处放置3min,加50mL水,加入0.3%淀粉溶液2mL,用0.1000mol•L-1Na2S2O3溶液滴定(发生:I2+2S2O32-═2I-+S4O62-)到终点时消耗12.00mL,试计算产品中Ca(IO3)2的质量分数(给出计算过程).

(1)若称取的I2质量为3.810g,为使I2充分氧化,则投料时KClO3的质量至少为3.675;同时生成的氯气体积为336mL(标准状况).
(2)用KOH溶液调节pH的目的是将KIO3•HIO3转变为KIO3.
(3)已知几种盐的溶解度(g/100g水)如下:
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KCl | 28.1 | 31.2 | 34.2 | 40.1 | 45.8 | 51.3 |
| Ca(IO3)2 | 0.119 | 0.195 | 0.3071 | 0.520 | 0.621 | 0.669 |
| 碘酸钙存在形态 | 无水盐 | 一水合物 | 六水合物 |
| 稳定时的温度区域 | >57.5℃ | 32-57.5℃ | <32℃ |
(4)准确称取产品0.6000g于烧标中,加1:1高氯酸20mL,微热溶解后,冷却,配成250.00mL溶液.移取上述溶液50.00mL置于250mL碘量瓶中,加入1:1高氯酸2mL、3gKI(足量)(发生:IO3-+5I-+6H+═3I2+3H2O),盖上瓶盖,暗处放置3min,加50mL水,加入0.3%淀粉溶液2mL,用0.1000mol•L-1Na2S2O3溶液滴定(发生:I2+2S2O32-═2I-+S4O62-)到终点时消耗12.00mL,试计算产品中Ca(IO3)2的质量分数(给出计算过程).
10.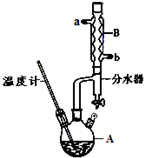 苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
(1)其制备方法为:
(2)已知:①
②苯甲酸在100℃会迅速升华
③无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
(3)实验步骤如下:
①在仪器A中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,仪器A的名称为三颈烧瓶,其容积最适合的是C(填选项前的字母).
A.25mL B.50mL C.100mL D.250mL
(2)制备苯甲酸乙酯时,最合适的加热方法是水浴加热,控制温度的目的是防止副反应的发生和苯甲酸升华.加入沸石的作用是防暴.
(3)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(4)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(5)步骤③有机层应从分液漏斗下口(填“上口”或“下口”)流出.加入Na2CO3的作用是除去硫酸和未反应的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是苯甲酸乙酯中混有未除净的苯甲酸,在受热至100℃时发生升华.加入氯化钙的目的是使产品中混有的乙醇形成难溶于水的CaCl2•6C2H5OH,过滤除去.
(6)计算本实验的产率为90.02%.
 苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.
苯甲酸乙酯(C9H10O2)是一种无色透明液体,不溶于水,稍有水果香味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体,溶剂等.(1)其制备方法为:

(2)已知:①
| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g•cm-3) |
| 苯甲酸 | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.8 | 0.7318 |
③无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
(3)实验步骤如下:
①在仪器A中加入12.20g苯甲酸,25mL 95%的乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装好仪器,控制温度在65~70℃加热回流2h.利用分水器不断分离除去反应生成的水,回流环己烷和乙醇.
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞,继续加热,至分水器中收集到的液体不再明显增加,停止加热.
③将仪器A内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性.用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,将滤液用蒸馏烧瓶进行分馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分.
④检验合格,测得产品体积为12.86mL.
回答下列问题:
(1)在该实验中,仪器A的名称为三颈烧瓶,其容积最适合的是C(填选项前的字母).
A.25mL B.50mL C.100mL D.250mL
(2)制备苯甲酸乙酯时,最合适的加热方法是水浴加热,控制温度的目的是防止副反应的发生和苯甲酸升华.加入沸石的作用是防暴.
(3)步骤①中使用分水器不断分离除去水的目的是使平衡不断地向正向移动.
(4)步骤②中应控制馏分的温度在C.
A.65~70℃B.78~80℃C.85~90℃D.215~220℃
(5)步骤③有机层应从分液漏斗下口(填“上口”或“下口”)流出.加入Na2CO3的作用是除去硫酸和未反应的苯甲酸;若Na2CO3加入不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是苯甲酸乙酯中混有未除净的苯甲酸,在受热至100℃时发生升华.加入氯化钙的目的是使产品中混有的乙醇形成难溶于水的CaCl2•6C2H5OH,过滤除去.
(6)计算本实验的产率为90.02%.
9.在25℃,101kPa下,1molH2充分燃烧生成液态水放热286kJ,下列说法中不正确的是( )
0 159238 159246 159252 159256 159262 159264 159268 159274 159276 159282 159288 159292 159294 159298 159304 159306 159312 159316 159318 159322 159324 159328 159330 159332 159333 159334 159336 159337 159338 159340 159342 159346 159348 159352 159354 159358 159364 159366 159372 159376 159378 159382 159388 159394 159396 159402 159406 159408 159414 159418 159424 159432 203614
| A. | 相同条件下,2mol H2完全燃烧时液态水放热572kJ | |
| B. | 相同条件下,2mol H2O完全分解吸收热量572kJ | |
| C. | 相同条件下,1mol H2充分燃烧生成气态水放热大于286kJ | |
| D. | 形成1mol H2O的化学键所释放的能量大于断裂lmol H2和0.5mol O2的化学键所吸收的总能量 |
 .
.