4.有机物的种类繁多,但其命名是有规则的.下列有机物用系统命名法命名正确的是( )
| A. |  1,4-二甲基丁烷 | B. | 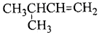 3-甲基丁烯 | C. | 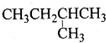 2-甲基丁烷 | D. | 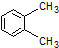 二甲苯 |
2.如表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题.
(1)单质的化学性质最不活沷的元素是Ne;
(2)氧的原子结构示意图是 ;
;
(3)形成化合物种类最多的元素是C;
(4)HF和H2O中,热稳定性较强的是HF;
(5)N和P中,原子半径较小的是N;
(6)常温下,会在浓硫酸中发生钝化的金属是Al;
(7)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),酸性最强的是HClO4(填“H2SO4”或“HClO4”).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
(2)氧的原子结构示意图是
 ;
;(3)形成化合物种类最多的元素是C;
(4)HF和H2O中,热稳定性较强的是HF;
(5)N和P中,原子半径较小的是N;
(6)常温下,会在浓硫酸中发生钝化的金属是Al;
(7)元素最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式),酸性最强的是HClO4(填“H2SO4”或“HClO4”).
20.下列物质燃烧时,不会造成大气污染的是( )
| A. | 石油 | B. | 农作物秸秆 | C. | 煤 | D. | 氢气 |
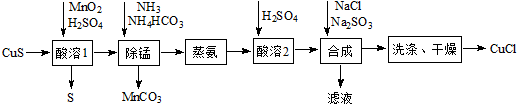
19.如图表示某物质发生的是( )
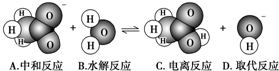

| A. | A | B. | B | C. | C | D. | D |
18. 苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:
苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:
反应过程: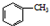 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$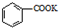 $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$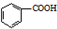
反应试剂、产物的物理常数:
注释:[1]100℃左右开始升华.
[2]苯甲酸在100g水中的溶解度为:4℃,0.18g;18℃,0.27g;75℃,2.2g.
按下列合成步骤回答问题:
Ⅰ.苯甲酸制备:
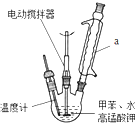
按如图在250mL三颈烧瓶中放入2.7mL甲苯和100mL水,控制100℃机械搅拌溶液,在石棉网上加热至沸腾.从冷
凝管上口分批加入8.5g高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约需4~5h,静置发现不再出
现分层现象时,停止反应.装置a的作用是将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率.写出并配平该反应化学方程式:

Ⅱ.分离提纯:
(1)除杂.将反应混合物加入一定量亚硫酸氢钠溶液使紫色褪去,此时反应的离子方程式为2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2 H2O.
(2)趁热过滤、热水洗涤.趁热过滤目的是除去二氧化锰并防止苯甲酸钾结晶析出造成损失.
(3)苯甲酸生成.合并实验(2)滤液和洗涤液,放在冰水浴中冷却,然后用浓盐酸酸化,至苯甲酸全部析出.将析出的苯甲酸减压过滤,得到滤液A和沉淀物B.沉淀物B用少量冷水洗涤,挤压去水分,把制得的苯甲酸放在水浴上干燥,得到粗产品C.
(4)粗产品提纯.将粗产品C进一步提纯,可用下列BD操作(填字母).
A.萃取分液 B.重结晶 C.蒸馏 D.升华
Ⅲ.产品纯度测定:称取1.220g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞(填写“甲基橙”或“酚酞”),然后用0.1000mol•L-1KOH溶液滴定,到达滴定终点时消耗KOH溶液24.00mL.产品中苯甲酸质量分数为96.00%.
0 159210 159218 159224 159228 159234 159236 159240 159246 159248 159254 159260 159264 159266 159270 159276 159278 159284 159288 159290 159294 159296 159300 159302 159304 159305 159306 159308 159309 159310 159312 159314 159318 159320 159324 159326 159330 159336 159338 159344 159348 159350 159354 159360 159366 159368 159374 159378 159380 159386 159390 159396 159404 203614
 苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:
苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等.实验室合成苯甲酸的原理、有关数据及装置示意图如下:反应过程:
 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$ $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$
反应试剂、产物的物理常数:
| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 密度(g/mL) | 溶解度(g) | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.4[1] | 248 | 1.2659 | 微溶[2] | 易溶 |
[2]苯甲酸在100g水中的溶解度为:4℃,0.18g;18℃,0.27g;75℃,2.2g.
按下列合成步骤回答问题:
Ⅰ.苯甲酸制备:
按如图在250mL三颈烧瓶中放入2.7mL甲苯和100mL水,控制100℃机械搅拌溶液,在石棉网上加热至沸腾.从冷
凝管上口分批加入8.5g高锰酸钾(加完后用少量水冲洗冷凝管内壁),继续搅拌约需4~5h,静置发现不再出
现分层现象时,停止反应.装置a的作用是将甲苯和水冷凝回流,防止甲苯的挥发而降低产品产率.写出并配平该反应化学方程式:

Ⅱ.分离提纯:
(1)除杂.将反应混合物加入一定量亚硫酸氢钠溶液使紫色褪去,此时反应的离子方程式为2MnO4-+3HSO3-+OH-=2MnO2↓+3SO42-+2 H2O.
(2)趁热过滤、热水洗涤.趁热过滤目的是除去二氧化锰并防止苯甲酸钾结晶析出造成损失.
(3)苯甲酸生成.合并实验(2)滤液和洗涤液,放在冰水浴中冷却,然后用浓盐酸酸化,至苯甲酸全部析出.将析出的苯甲酸减压过滤,得到滤液A和沉淀物B.沉淀物B用少量冷水洗涤,挤压去水分,把制得的苯甲酸放在水浴上干燥,得到粗产品C.
(4)粗产品提纯.将粗产品C进一步提纯,可用下列BD操作(填字母).
A.萃取分液 B.重结晶 C.蒸馏 D.升华
Ⅲ.产品纯度测定:称取1.220g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞(填写“甲基橙”或“酚酞”),然后用0.1000mol•L-1KOH溶液滴定,到达滴定终点时消耗KOH溶液24.00mL.产品中苯甲酸质量分数为96.00%.
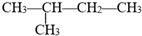 用系统命名法命名的名称是2-甲基丁烷,它的一氯代物有4种,若它是用烯烃和氢气加成而得到,则烯烃可能的结构简式是:CH2=(CH3)C-CH2-CH3;(CH3)2C=CH-CH3;(CH3)2CH-CH=CH2.
用系统命名法命名的名称是2-甲基丁烷,它的一氯代物有4种,若它是用烯烃和氢气加成而得到,则烯烃可能的结构简式是:CH2=(CH3)C-CH2-CH3;(CH3)2C=CH-CH3;(CH3)2CH-CH=CH2.