19.将过氧化钠投入FeCl2溶液中,可观察到的实验现象是( )
| A. | 有白色沉淀生成 | B. | 没有沉淀生成 | ||
| C. | 有红褐色沉淀生成 | D. | 有无色气体产生 |
18.根据实验室制取某干燥气体的装置图(如图所示),判断气体发生装置中的药品可能是( )
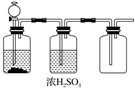

| A. | FeS和稀H2SO4 | B. | 加热NaCl和浓H2SO4制HCl | ||
| C. | 大理石和稀盐酸 | D. | MnO2和浓盐酸 |
15.下列叙述正确的是( )
| A. | 所有的物质中都含有化学键 | |
| B. | 含有非极性键的化合物不一定是共价化合物 | |
| C. | 反应物总能量低于生成物总能量的反应一定是吸热反应 | |
| D. | 由非金属元素构成的化合物一定是共价化合物 |
14.将铁和铜混合均匀并平均分成四等份,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO).
计算:
(1)硝酸的浓度为多少?
(2)③中溶解的Cu的质量为多少?
(3)④中的V为多少?
0 159198 159206 159212 159216 159222 159224 159228 159234 159236 159242 159248 159252 159254 159258 159264 159266 159272 159276 159278 159282 159284 159288 159290 159292 159293 159294 159296 159297 159298 159300 159302 159306 159308 159312 159314 159318 159324 159326 159332 159336 159338 159342 159348 159354 159356 159362 159366 159368 159374 159378 159384 159392 203614
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
(1)硝酸的浓度为多少?
(2)③中溶解的Cu的质量为多少?
(3)④中的V为多少?
 由C与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
由C与水反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.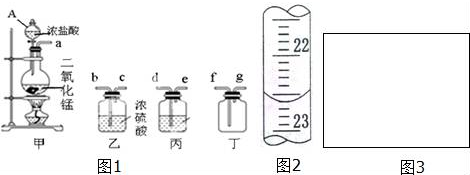
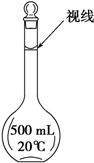 实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有: