13.几种有机化合物的结构简式如下:①CH3-CHO;②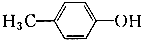 ;③
;③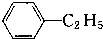 ;④CH3COOC2H5;⑤
;④CH3COOC2H5;⑤ ;⑥
;⑥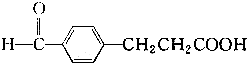 ,有关上述有机化合物的类别叙述正确的是( )
,有关上述有机化合物的类别叙述正确的是( )
 ;③
;③ ;④CH3COOC2H5;⑤
;④CH3COOC2H5;⑤ ;⑥
;⑥ ,有关上述有机化合物的类别叙述正确的是( )
,有关上述有机化合物的类别叙述正确的是( )| A. | ①醛,②酚,③环烷烃,④酯,⑤羧酸,⑥酯 | |
| B. | ①醇,②酚,③芳香烃,④酚,⑤芳香烃,⑥羧酸 | |
| C. | ①醛,②醇,③芳香烃,④羧酸,⑤羧酸,⑥醛 | |
| D. | ①醛,②酚,③芳香烃,④酯,⑤羧酸,⑥羧酸 |
12.只给出下列物理量a和b,不能求出物质的量的是( )
| 选项 | 物理量a | 物理量b |
| A | 物质中的粒子数 | 阿伏加德罗常数 |
| B | 标准状况下的气体摩尔体积 | 标准状况下的气体体积 |
| C | 固体的体积 | 固体的密度 |
| D | 物质的摩尔质量 | 物质的质量 |
| A. | A | B. | B | C. | C | D. | D |
11.下列各组溶液中,c(NO3-)与200mL0.2mol•L-1Na2SO4溶液中的c(SO42-)相同的是( )
| A. | l00mL0.4 mol•L-1KNO3溶液 | B. | 100mL0.2mol•L-1Cu(NO3)2溶液 | ||
| C. | 200mLO.l mol•L-1Fe(NO3)2溶液 | D. | 400mLO.l mol•L-1Al(NO3)3溶液 |
10.下列气体中不能用浓硫酸干燥的是( )
| A. | NH3 | B. | N2 | C. | CO2 | D. | H2 |
9.下列分散系中,分散质较子半径最小的是( )
| A. | 烟 | B. | 雾 | C. | 食用油滴入水中 | D. | KNO3溶于水 |
8.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法中,正确的是( )
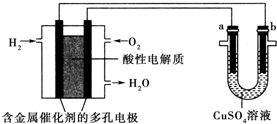

| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | 此装置用于铁表面镀铜时,a为铁 | |
| C. | a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | a、b两极均是石墨时,在相同条件下,a极产生的气体与电池中消耗的H2体积相等 |
7.设NA为阿伏加德罗常数值.下列有关说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 1molN2与4molH2反应生成的NH3分子数为2NA | |
| C. | 1molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 5.6LCO2气体中含有的氧原子数为0.5NA |
6.电解硫酸铜溶液要达到如下三个要求:①阳极质量减小 ②阴极质量增加 ③电解过程中Cu2+浓度不变,则可选用的电极是( )
| A. | 石墨作阳极,铁作阴极 | |
| B. | 粗铜(含Fe、Ni、Zn)作阳极,纯铜作阴极 | |
| C. | 纯铜作阳极,铁作阴极 | |
| D. | 铁作阳极,纯铜作阴极 |
5.下面列出了用惰性电极电解不同物质的电极反应式,其中错误的是( )
| A. | 电解饱和BaCl2溶液 阴极:Ba2++2e-=Ba | |
| B. | 电解Cu(NO3)2溶液 阴极:Cu2++2e-=Cu | |
| C. | 电解熔融NaCl阴极:Na++e-=Na | |
| D. | 电解NaOH溶液 阳极:4OH--4e-=2H2O+O2↑ |
4.回收利用印刷电路板上的铜制备铜的化合物,实现资源的再利用.
(1)回收利用印刷电路板上的铜制备CuCl2.
实验室模拟回收过程如下:
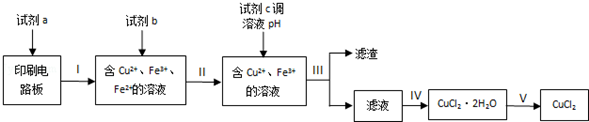
已知部分物质开始沉淀和沉淀完全时的pH如下表:
请回答下列问题:
①步骤Ⅲ的操作名称是过滤.
②下列试剂中,可以作为试剂a的是C.
A.HNO3溶液 B.Fe2(SO4)3溶液 C.FeCl3溶液
③若不加试剂b,直接加入试剂c调节溶液pH,是否可行?否(填“是”或“否”),理由是不能除去Fe2+,影响所得CuCl2纯度.
(2)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜.
已知:2H2O2(l)=2H2O (l)+O2(g)△H1=-196kJ/mol
H2O(l)=H2(g)+$\frac{1}{2}$O2(g)△H2=+286kJ/mol
Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)△H3=+64kJ/mol
则Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l)△H=-320kJ/mol.
(3)将反应Cu+H2O2+H2SO4=CuSO4+2H2O设计成原电池,其正极电极反应式是H2O2+2H++2e-=2H2O.
(4)若用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,假设印刷电路板中其他成分不与酸反应,欲制取3mol纯净的硫酸铜,需要0.5mol/L的硝酸溶液的体积是4L.
0 159185 159193 159199 159203 159209 159211 159215 159221 159223 159229 159235 159239 159241 159245 159251 159253 159259 159263 159265 159269 159271 159275 159277 159279 159280 159281 159283 159284 159285 159287 159289 159293 159295 159299 159301 159305 159311 159313 159319 159323 159325 159329 159335 159341 159343 159349 159353 159355 159361 159365 159371 159379 203614
(1)回收利用印刷电路板上的铜制备CuCl2.
实验室模拟回收过程如下:

已知部分物质开始沉淀和沉淀完全时的pH如下表:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.4 | 8.0 |
①步骤Ⅲ的操作名称是过滤.
②下列试剂中,可以作为试剂a的是C.
A.HNO3溶液 B.Fe2(SO4)3溶液 C.FeCl3溶液
③若不加试剂b,直接加入试剂c调节溶液pH,是否可行?否(填“是”或“否”),理由是不能除去Fe2+,影响所得CuCl2纯度.
(2)用H2O2和硫酸共同浸泡印刷电路板制备硫酸铜.
已知:2H2O2(l)=2H2O (l)+O2(g)△H1=-196kJ/mol
H2O(l)=H2(g)+$\frac{1}{2}$O2(g)△H2=+286kJ/mol
Cu(s)+H2SO4(aq)=CuSO4(aq)+H2(g)△H3=+64kJ/mol
则Cu(s)+H2O2(l)+H2SO4(aq)=CuSO4(aq)+2H2O(l)△H=-320kJ/mol.
(3)将反应Cu+H2O2+H2SO4=CuSO4+2H2O设计成原电池,其正极电极反应式是H2O2+2H++2e-=2H2O.
(4)若用硝酸和硫酸共同浸泡印刷电路板制备硫酸铜,假设印刷电路板中其他成分不与酸反应,欲制取3mol纯净的硫酸铜,需要0.5mol/L的硝酸溶液的体积是4L.