18.下列实验操作中,错误的是( )
| A. | 利用丁达尔效应区分溶液和胶体 | |
| B. | 向沸水中滴加饱和的FeCl3溶液制取Fe(OH)3胶体 | |
| C. | 用渗析的方法除去胶体中的离子或分子 | |
| D. | 用滤纸过滤除去溶液中的胶体粒子 |
17.下列电离方程式,书写正确的是( )
| A. | Al2(SO4)3=2Al3++3SO42- | B. | AlCl3=Al3++Cl3- | ||
| C. | NaHCO3=Na++H++CO32- | D. | KMnO4=K++Mn7++4O2- |
14.某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:
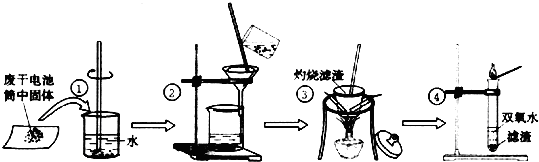
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是溶解;操作②的名称是过滤;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、坩埚、泥三角 和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(碳).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2.
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
0 159178 159186 159192 159196 159202 159204 159208 159214 159216 159222 159228 159232 159234 159238 159244 159246 159252 159256 159258 159262 159264 159268 159270 159272 159273 159274 159276 159277 159278 159280 159282 159286 159288 159292 159294 159298 159304 159306 159312 159316 159318 159322 159328 159334 159336 159342 159346 159348 159354 159358 159364 159372 203614

查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
(1)操作①的名称是溶解;操作②的名称是过滤;
(2)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、坩埚、泥三角 和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为C(碳).
(3)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为MnO2.
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中,加入硝酸酸化的硝酸银溶液 | 产生白色沉淀 | 含有Cl- |
| 2.检验NH4+ | 取少许滤液于试管中,加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ k |
| 3.检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
 )是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
)是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基香草醛分子中两种含氧官能团的名称:酚羟基、醛基,核磁共振氢谱显示该分子中有7种不同类型的氢原子.
 ,属于取代反应(填反应类型).
,属于取代反应(填反应类型). .
. .
. )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件). $→_{催化剂△}^{H_{2}}$
$→_{催化剂△}^{H_{2}}$ $→_{光照}^{Br_{2}}$
$→_{光照}^{Br_{2}}$
 .
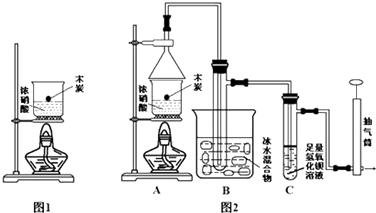
.
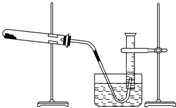 某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
某学生利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下: