3..室温时,下列各组中的物质分别与过量NaOH溶液反应,能生成5种盐的是( )
| A. | Al2O3、SO2、CO2、SO3 | B. | CO2、Cl2、CaO、SO3 | ||
| C. | Cl2、Al2O3、SO2、SO3 | D. | SiO2、CO2、CO、Cl2 |
2.下列仪器不能用酒精灯直接加热的是( )
①烧杯 ②坩埚 ③烧瓶 ④试管 ⑤锥形瓶 ⑥蒸发皿 ⑦容量瓶 ⑧表面皿.
①烧杯 ②坩埚 ③烧瓶 ④试管 ⑤锥形瓶 ⑥蒸发皿 ⑦容量瓶 ⑧表面皿.
| A. | ①③⑤⑦⑧ | B. | ①③④⑤⑦ | C. | ④⑦⑧ | D. | ②③⑤⑦⑧ |
1.下列各组物质中,只含有共价键的是( )
| A. | NH3、CO2 | B. | CaO、HCl | C. | Na2S、MgO | D. | H2O、Na2O2 |
20.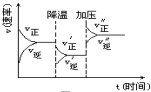 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 逆反应是放热反应 | B. | 正反应是放热反应 | ||
| C. | 若A、B是气体,则D一定是气体 | D. | A、B、C、D均为气体 |
19.有FeO、Fe2O3的混合物若干克,在足量氢气中加热充分反应,冷却后称得剩余固体比原混合物减轻了8克;将等质量的原混合物与盐酸反应,欲使之完全溶解,需要的盐酸的物质的量至少为( )
| A. | 0.5mol | B. | 0.1mol | C. | 2mol | D. | 1mol |
18.升高温度时,化学反应速率加快原因的合理解释是( )
| A. | 该化学反应的过程是吸热的 | |
| B. | 该化学反应的过程是放热的 | |
| C. | 分子运动速率加快,使反应物分子的碰撞机会增多 | |
| D. | 反应物分子的能量增加,活化分子百分数增加,有效碰撞次数增多 |
17.稀氨水中存在电离平衡:NH3•H2O?NH4++OH-,若要使平衡正向移动,同时使c(OH-)减小,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤通入HCl ⑥加入少量MgSO4固体.
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑤ | D. | ②④⑤⑥ |
16.向明矾水溶液中加入一种溶液,首先能使胶体凝聚而沉淀,继续滴加该溶液时,沉淀又逐渐消失,这种溶液是( )
| A. | BaCl2溶液 | B. | 盐酸 | C. | 蒸馏水 | D. | 烧碱溶液 |
15.下列现象或事实可用同一原理解释的是( )
| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度降低 | |
| B. | 氯水和活性炭使红墨水褪色 | |
| C. | 漂白粉和钠长期暴露在空气中变质 | |
| D. | 氯水和过氧化钠使品红褪色 |
14.将A与B的混合物15mol放人容积为2L的密闭容器里,在一定条件下发生反应:2A(g)+3B(g)?C(g)+2D(g),经过15min达到平衡,达平衡时容器内的压强是反应前的$\frac{4}{5}$.则以B气体的浓度变化表示的反应速率是( )
0 159170 159178 159184 159188 159194 159196 159200 159206 159208 159214 159220 159224 159226 159230 159236 159238 159244 159248 159250 159254 159256 159260 159262 159264 159265 159266 159268 159269 159270 159272 159274 159278 159280 159284 159286 159290 159296 159298 159304 159308 159310 159314 159320 159326 159328 159334 159338 159340 159346 159350 159356 159364 203614
| A. | 0.15mol•L-1•min-1 | B. | 0.3mol•L-1•min-1 | ||
| C. | 0.45mol•L-1•min-1 | D. | 0.6mol•L-1•min-1 |