10.下列药品和装置合理且能完成相应实验的是( )
| A. | 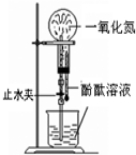 喷泉实验 | B. | 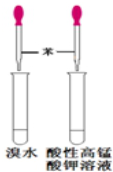 验证苯中是否含有碳碳双键 | ||
| C. | 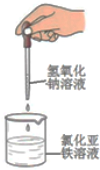 制备氢氧化亚铁 | D. | 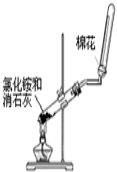 实验室制取并收集氨气 |
9.在化学实验时必须注意安全操作,避免意外伤害,下列实验操作或事故处理中不正确的是( )
| A. | 在点燃易燃气体前,必须检验气体的纯度 | |
| B. | 在稀释浓硫酸时,应将浓硫酸用玻璃棒引流慢慢注入水中 | |
| C. | 浓硫酸有腐蚀性,沾到皮肤上,应用较多的水冲洗,再涂上碳酸氢钠稀溶液 | |
| D. | 不得点燃添满酒精的酒精灯 |
7.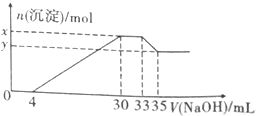 在100ml含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol•L-1NaOH溶液,所加NaOH溶液的体积(ml)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
在100ml含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol•L-1NaOH溶液,所加NaOH溶液的体积(ml)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
 在100ml含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol•L-1NaOH溶液,所加NaOH溶液的体积(ml)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
在100ml含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol•L-1NaOH溶液,所加NaOH溶液的体积(ml)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )| A. | x-y=2×10-3mol | B. | 原溶液的pH=2 | ||
| C. | 原溶液中n(Cu2+)=0.025mol | D. | 原溶液中c(NH4+)=7.5×10-3mol•L-1 |
6.向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色.再向反应后的混合物中不断通入SO2气体,溶液逐渐变为无色.下列分析正确的是( )
| A. | 滴加KI溶液时,当有2molI-参加反应,则生成1mol白色沉淀 | |
| B. | 通入SO2后溶液逐渐变成无色,体现了SO2的氧化性 | |
| C. | 通入SO2时,SO2与I2反应,I2作还原剂,H2SO4是氧化产物 | |
| D. | 上述实验条件下,物质的还原性:Cu+>I->SO2 |
4.部分果蔬中含有下列成分:
已知:
①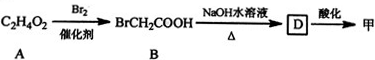
②1mol乙消耗NaHCO3 的物质的量是甲的2倍
③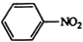 $\stackrel{Fe,HCl}{→}$
$\stackrel{Fe,HCl}{→}$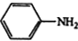 $→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$
$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$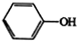
回答下列问题:
(1)甲可由已知①得到.
①甲中含有不饱和键的官能团名称为羧基.
②A→B为取代反应,A的结构简式为CH3COOH.
③B→D的化学方程式为BrCH2COOH+2NaOH$→_{△}^{H_{2}O}$HOCH2COONa+NaBr+H2O.
(2)乙在一定条件下生成链状酯类有机高分子化学物的化学方程式为n HOOCCH(OH)COOH$\stackrel{一定条件}{→}$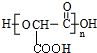 +(n-1)H2O.
+(n-1)H2O.
(3)由丙经下列途径可得一种重要的医药和香料中间体J(部分反应条件略去):
丙$→_{催化剂,△}^{H_{2}}$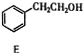 $\stackrel{经两步}{→}$
$\stackrel{经两步}{→}$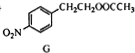 $→_{(2)H+,△}^{(1)Fe,HCl}$$\stackrel{{C}_{8}{H}_{11}NO}{H}$$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$J
$→_{(2)H+,△}^{(1)Fe,HCl}$$\stackrel{{C}_{8}{H}_{11}NO}{H}$$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$J
①用化学方法除去E中残留的少量丙(室温时E和丙呈液态,忽略它们在水中的溶解),第1步加入试剂的名称为新制氢氧化铜或银氨溶液,第2、3 步操作分别是过滤、分液.
②经E→G→H保护的官能团是羟基,可以表征有机化合物中存在何种官能团的仪器是红外光谱仪.
③J的同分异构体中在核磁共振氢谱上显示为两组峰,峰面积比为3:2的链状且不存在支链的异构体共有8种(不含立体异构),其中某异构体L中的官能团都能与H2 发生加成反应,则L的结构简式为CH3CH2COC≡CCOCH2CH3或CH3COCH2C≡CCH2COCH3(只写一种).
| 甲 | 乙 | 丙 |
| 柚子 | 黄瓜 | 脐橙 |
| HOCH2COOH | C3H4O5 | 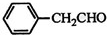 |
①
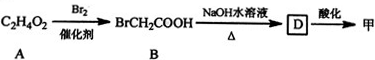
②1mol乙消耗NaHCO3 的物质的量是甲的2倍
③
 $\stackrel{Fe,HCl}{→}$
$\stackrel{Fe,HCl}{→}$ $→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$
$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$
回答下列问题:
(1)甲可由已知①得到.
①甲中含有不饱和键的官能团名称为羧基.
②A→B为取代反应,A的结构简式为CH3COOH.
③B→D的化学方程式为BrCH2COOH+2NaOH$→_{△}^{H_{2}O}$HOCH2COONa+NaBr+H2O.
(2)乙在一定条件下生成链状酯类有机高分子化学物的化学方程式为n HOOCCH(OH)COOH$\stackrel{一定条件}{→}$
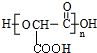 +(n-1)H2O.
+(n-1)H2O.(3)由丙经下列途径可得一种重要的医药和香料中间体J(部分反应条件略去):
丙$→_{催化剂,△}^{H_{2}}$
 $\stackrel{经两步}{→}$
$\stackrel{经两步}{→}$ $→_{(2)H+,△}^{(1)Fe,HCl}$$\stackrel{{C}_{8}{H}_{11}NO}{H}$$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$J
$→_{(2)H+,△}^{(1)Fe,HCl}$$\stackrel{{C}_{8}{H}_{11}NO}{H}$$→_{(2)H_{2}O,H+,△}^{(1)NaNO_{2},HCl}$J①用化学方法除去E中残留的少量丙(室温时E和丙呈液态,忽略它们在水中的溶解),第1步加入试剂的名称为新制氢氧化铜或银氨溶液,第2、3 步操作分别是过滤、分液.
②经E→G→H保护的官能团是羟基,可以表征有机化合物中存在何种官能团的仪器是红外光谱仪.
③J的同分异构体中在核磁共振氢谱上显示为两组峰,峰面积比为3:2的链状且不存在支链的异构体共有8种(不含立体异构),其中某异构体L中的官能团都能与H2 发生加成反应,则L的结构简式为CH3CH2COC≡CCOCH2CH3或CH3COCH2C≡CCH2COCH3(只写一种).
2.短周期主族元素 X、Y、Z、W、Q 的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z 的单质能溶于 W 的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液.下列说法不正确的是( )
0 159159 159167 159173 159177 159183 159185 159189 159195 159197 159203 159209 159213 159215 159219 159225 159227 159233 159237 159239 159243 159245 159249 159251 159253 159254 159255 159257 159258 159259 159261 159263 159267 159269 159273 159275 159279 159285 159287 159293 159297 159299 159303 159309 159315 159317 159323 159327 159329 159335 159339 159345 159353 203614
| A. | 原子半径的大小顺序为 W>Q>Z>X>Y | |
| B. | 元素 Y 与 W 对应氢化物的沸点 H2Y>H2W | |
| C. | 元素 X 与 Y 可以形成 5 种以上的化合物 | |
| D. | 元素 Q 的最高价氧化物对应的水化物酸性比 W 的强 |
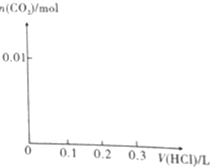 (1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.
(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.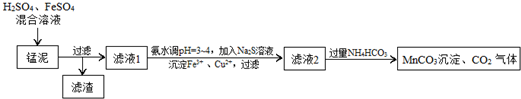
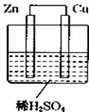 如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )
如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )