10.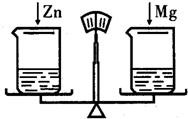 在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )
在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )
 在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )
在托盘天平的两托盘上各放一只烧杯,分别注人足量的稀盐酸,天平平衡.向左边烧杯中加入10克金属锌,向右边烧杯中加入10克金属镁,当反应停止后,天平指针的指向是( )| A. | 分度盘的左边 | B. | 分度盘的中间 | ||
| C. | 分度盘的右边 | D. | 三种情况都有可能 |
9. 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:
回答下列问题:
(1)物质的量浓度均为0.1mol•L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO
d.NaHCO3; pH由小到大的排列顺序是(填序号)a<d<c<b.
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,
下列表达式的数据变大的是BD.
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)•c(OH-)
D.c(OH-)/c(H+) E.c(H+)•c(CH3COO-)/c(CH3COOH)
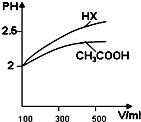
(3)体积均为100ml pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX)> Ka(CH3COOH)(填>、<或=).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中自由离子浓度的从大到小
的关系为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
 已知25℃时部分弱电解质的电离平衡常数数据如表:
已知25℃时部分弱电解质的电离平衡常数数据如表:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol•L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO
d.NaHCO3; pH由小到大的排列顺序是(填序号)a<d<c<b.
(2)常温下,0.1mol•L-1的CH3COOH溶液加水稀释过程中,
下列表达式的数据变大的是BD.
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)•c(OH-)
D.c(OH-)/c(H+) E.c(H+)•c(CH3COO-)/c(CH3COOH)
(3)体积均为100ml pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,
则Ka(HX)> Ka(CH3COOH)(填>、<或=).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中自由离子浓度的从大到小
的关系为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18.
7.下列各组分子中,中心原子杂化轨道的类型不相同的是( )
| A. | CO2与SO2 | B. | CH4与NH3 | C. | SO3与BF3 | D. | H2S与CCl4 |
6. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
(1)①写出工业合成氨的化学方程式N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
②由上表数据可知该反应为放热反应,理由是随温度升高,反应的平衡常数K减小.
③理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
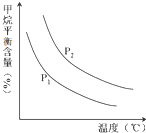
(2)原料气H2可通过反应 CH4(g)+H2O (g)═CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的 $\frac{n({H}_{2}O)}{n(C{H}_{4})}$ 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)═CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该反应平衡常数的表达式为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n (CO):n (H2O):n (CO2):n (H2)=1:1:1:1.
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
②由上表数据可知该反应为放热反应,理由是随温度升高,反应的平衡常数K减小.
③理论上,为了增大平衡时H2的转化率,可采取的措施是ad.(填序号)
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2可通过反应 CH4(g)+H2O (g)═CO(g)+3H2(g) 获取,已知该反应中,当初始混合气中的 $\frac{n({H}_{2}O)}{n(C{H}_{4})}$ 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是:P1<P2(填“>”、“=”或“<”).
②该反应为吸热反应(填“吸热”或“放热”).
(3)原料气H2还可通过反应CO(g)+H2O(g)═CO2 (g)+H2(g) 获取.
①T℃时,向容积固定为5L的容器中充入1mol水蒸气和1mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则平衡时CO的转化率为60%,该反应平衡常数的表达式为2.25.
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是cd(填序号).
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n (CO):n (H2O):n (CO2):n (H2)=1:1:1:1.
5.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为14.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍.下列说法不正确的是( )
| A. | X的氢化物溶液与其最高价氧化物对应的水化物溶液的酸碱性相反 | |
| B. | Y的氧化物既可与强酸反应又可与强碱反应,并可用来制作耐火材料 | |
| C. | X和Z的最高价氧化物对应的水化物的浓溶液都是具有强氧化性的酸 | |
| D. | 因为Z的氢化物相对分子质量大于X的氢化物,其熔沸点较高 |
4.对于反应CO(g)+H2O(g)?CO2(g)+H2(g)△H=-aKJ/mol,在其他条件不变的情况下,下列说法正确的是( )
| A. | 1mol CO(g)和1molH2O(g)充分反应,放出的热量为aKJ | |
| B. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| C. | 升高温度,速率加快,反应放出的热量不变 | |
| D. | 若将该反应设计为原电池,反应放出的热量不变 |
3.下列有关用途的说法中,错误的是( )
| A. | 液态钠可用作核反应堆的传热介质 | |
| B. | 在过渡元素中寻找半导体材料 | |
| C. | 考古时利用l4C测定一些文物的年代 | |
| D. | 235U是一种重要核燃料 |
1.某元素A有两种天然同位素35A和37A,35A和37A原子百分数分别为75%和25%,则此元素的近似相对原子质量是( )
0 159153 159161 159167 159171 159177 159179 159183 159189 159191 159197 159203 159207 159209 159213 159219 159221 159227 159231 159233 159237 159239 159243 159245 159247 159248 159249 159251 159252 159253 159255 159257 159261 159263 159267 159269 159273 159279 159281 159287 159291 159293 159297 159303 159309 159311 159317 159321 159323 159329 159333 159339 159347 203614
| A. | 35 | B. | 37 | C. | 36 | D. | 35.5 |
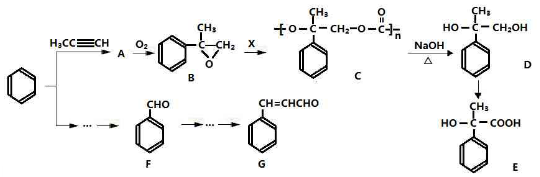
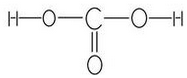 .
. .
.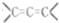 的有机物不能稳定存在)
的有机物不能稳定存在)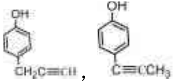 .
.