18.下列离子方程式书写正确的是( )
| A. | 向碳酸氢钙溶液中加人过量氢氧化钠Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 金属铝溶于盐酸中:Al+2H+═Al3++H2↑ | |
| C. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | CuSO4溶液中加入少量Ba(OH)2溶液:SO42-+Ba2+═BaSO4↓ |
17.下列反应中硫酸既不表现氧化性且又不表现还原性的是( )
| A. | 2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑ | |
| B. | 2H2SO4(浓)+C$\frac{\underline{\;\;△\;\;}}{\;}$2SO2↑+CO2↑+2H2O | |
| C. | H2SO4(稀)+Zn═ZnSO4+H2↑ | |
| D. | H2SO4+Na2SO3═Na2SO4+H2O+SO2↑ |
16.下列分离物质的方法中,根据微粒大小进行分离的是( )
| A. | 萃取 | B. | 蒸馏 | C. | 分液 | D. | 渗析 |
15.对于密闭容器中进行的反应:N2+O2=2NO,下列条件中哪些能加快该反应速率的(假定改变下列条件时温度不变)( )
| A. | 压强不变,充入Ne使体积增大 | B. | 体积不变充入N2使压强增大 | ||
| C. | 体积不变充入He气使压强增大 | D. | 减小压强使体积增大 |
14.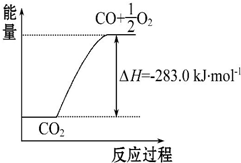 已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
下列说法正确的是( )
 已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
下列说法正确的是( )
| A. | 通常状况下,氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 由①可知,1 mol CO(g)和$\frac{1}{2}$mol O2(g)反应生成1 mol CO2(g),放出283.0 kJ的热量 | |
| C. | 可用右图表示2CO2(g)═2CO(g)+O2(g)反应过程中的能量变化关系 | |
| D. | 分解1 mol H2O(g),其反应热为-241.8 KJ |
13.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量;②1molCl2分子中化学键断裂时需要吸收243kJ的能量;③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量.下列叙述正确的是( )
| A. | 氢气和氯气反应生成氯化氢气体的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-183kJ | |
| B. | 氢气与氯气反应生成4.48L氯化氢气体,反应的△H=-183kJ/mol | |
| C. | 氢气与氯气反应生成2mol氯化氢气体,反应的△H=+183kJ/mol | |
| D. | 氢气与氯气反应生成氯化氢气体放出183KJ的热量时,转移电子物质的量为2 mol |
12.肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气.已知:N2(g)+2O2(g)=N2O4(g)△H=+8.7kJ/mol;N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534.0kJ/mol.下列表示肼跟N2O4反应的热化学方程式,正确的是( )
0 159132 159140 159146 159150 159156 159158 159162 159168 159170 159176 159182 159186 159188 159192 159198 159200 159206 159210 159212 159216 159218 159222 159224 159226 159227 159228 159230 159231 159232 159234 159236 159240 159242 159246 159248 159252 159258 159260 159266 159270 159272 159276 159282 159288 159290 159296 159300 159302 159308 159312 159318 159326 203614
| A. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-542.7kJ/mol | |
| B. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1059.3kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)△H=-1076.7kJ/mol | |
| D. | N2H4(g)+$\frac{1}{2}$N2O4(g)=$\frac{3}{2}$N2(g)+2H2O(g)△H=-1076.7kJ/mol |
