15.氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用.请回答下列问题.
(1)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(2)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,沸点高低的原因是:结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4.
②NH3和PH3比较,沸点高低的原因是:NH3分子间还存在氢键作用,因此NH3的沸点高于PH3.
(1)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(2)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
①CH4和SiH4比较,沸点高低的原因是:结构相似时,相对分子质量越大,分子间作用力越大,因此CH4的沸点低于SiH4.
②NH3和PH3比较,沸点高低的原因是:NH3分子间还存在氢键作用,因此NH3的沸点高于PH3.
14.常温下三氯化氮(NCl3)是一种淡黄色液体.以下关于NCl3的说法中,正确的是( )
| A. | 分子中 N-Cl键是非极性键 | B. | 分子中不存在孤对电子 | ||
| C. | 三氯化氮分子结构呈三角锥形 | D. | 因N-Cl 键键能大,它的沸点高 |
13.下列分子中,中心原子是sp1杂化的是( )
| A. | BeCl2 | B. | H2O | C. | CH4 | D. | BF3 |
12.下列物质的性质与氢键无关的是( )
| A. | 冰的密度比液态水的密度小 | B. | NH3易液化 | ||
| C. | NH3比PH3分子稳定 | D. | 乙醇以任意比例溶于水 |
11.以下能级符号不正确的是( )
| A. | 3s | B. | 3p | C. | 3d | D. | 2d |
10.首次将量子化概念应用到原子结构,并解释了原子的稳定性的科学家是( )
0 159117 159125 159131 159135 159141 159143 159147 159153 159155 159161 159167 159171 159173 159177 159183 159185 159191 159195 159197 159201 159203 159207 159209 159211 159212 159213 159215 159216 159217 159219 159221 159225 159227 159231 159233 159237 159243 159245 159251 159255 159257 159261 159267 159273 159275 159281 159285 159287 159293 159297 159303 159311 203614
| A. | 道尔顿 | B. | 爱因斯坦 | C. | 玻尔 | D. | 卢瑟福 |
 ,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: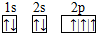 .
.
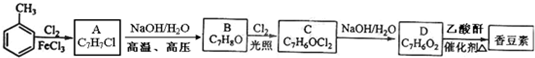
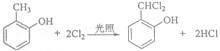 .
.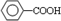 (写结构简式).
(写结构简式).