17.乙烯分子中同一个碳原子上的C-H键的键角为( )
| A. | 120° | B. | 104°30′ | C. | 109°28′ | D. | 60° |
14. (1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
(1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
复分解反应存在这样一个规律:一种较强酸(或碱性较强的物质)可以自发地反应生成较弱酸(或碱性较弱的物质).照该规律,请判断下列反应不能成立的是CD (填编号).
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前述信息判断,浓度均为0.05mol•L-1的下列六种物质的溶液中,pH最小的是⑤ (填编号);将各溶液分别稀释100倍,pH变化最小的是① (填编号).
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-.
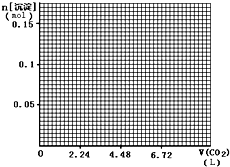
(4)标准状况下,向1L含NaOH、Ca(OH)2各0.1mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图.
 (1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:
(1)已知:在常温下,浓度均为0.1mol•L-1的下列六种溶液的pH:| 溶质 | CH3CO ONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
(2)根据前述信息判断,浓度均为0.05mol•L-1的下列六种物质的溶液中,pH最小的是⑤ (填编号);将各溶液分别稀释100倍,pH变化最小的是① (填编号).
①C6H5OH ②CH3COOH ③HCN ④HClO ⑤H2SO4 ⑥HClO4
(3)根据前述信息,写出将过量的氯气通入到少量的碳酸钠溶液中反应的离子方程式:Cl2+H2O+2CO32-=2HCO3-+Cl-+ClO-.
(4)标准状况下,向1L含NaOH、Ca(OH)2各0.1mol的溶液中不断通入CO2至过量,请画出产生的沉淀的物质的量(mol)随CO2通入体积(L)的变化趋势图.
12.某溶液可能含有大量CO32-、S2-、SO32-、SO42-、NO3-、NO2-、OH-等阴离子.为检测上述阴离子,某研究性小组设计了下列实验:
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊.
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生.
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色.
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生.
下列说法正确的是( )
①取少量吸收液于试管中,加入过量的稀盐酸,产生淡黄色浑浊和气体,将所得的气体依次通入品红溶液、足量酸性KMnO4溶液和澄清石灰水,品红褪色,石灰水变浑浊.
②另取少量待测液于试管中,加入过量的KClO3固体、AgNO3和稀硝酸,有白色沉淀产生.
③另取少量待测液于试管中,酸化后再加入淀粉KI溶液,呈蓝色.
④另取少量待测液于试管中,加入足量的BaCl2溶液和稀盐酸,有白色沉淀产生.
下列说法正确的是( )
| A. | 由①可推测溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推测溶液中一定含大量NO2- | |
| C. | 由③可推测溶液中一定含大量NO3- | |
| D. | 由实验④难以推测溶液中一定含大量SO42- |
11.下列反应的离子方程式不正确的是( )
| A. | Ba(OH)2溶液中加入过量Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ | |
| B. | FeCl3溶液中加少量Na2S溶液:2Fe3++S2-=2Fe2++S↓ | |
| C. | 向硫酸铜溶液中加入过量氨水:Cu2++2NH3•H2O=Cu(OH)2↓+2NH4+ | |
| D. | 向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-=CO32-+CaCO3↓+2H2O |
8.三种常见元素结构信息如下表,试根据信息回答有关问题:
(1)写出B原子的基态电子排布式1s22s22p63s23p4;
(2)用氢键表示式写出A的氢化物溶液中存在的所有氢键N-H…N-N-H…O-O-H…N-O-H…O-;A的氢化物分子结合一个H+形成阳离子后,其键角变大(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,
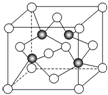
(4)科学家通过X射线推测胆矾中微粒间的作用力,胆矾的结构示意图
可简单表示如图1:
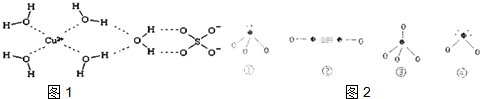
则胆矾晶体中含有ABCE
A.配位键 B.离子键 C.极性共价键 D.金属键 E.氢键F.非极性共价键
(5)下列分子结构图2中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.在以上分子中,中心原子采用sp3杂化形成化学键是①③④(填写序号).
0 159115 159123 159129 159133 159139 159141 159145 159151 159153 159159 159165 159169 159171 159175 159181 159183 159189 159193 159195 159199 159201 159205 159207 159209 159210 159211 159213 159214 159215 159217 159219 159223 159225 159229 159231 159235 159241 159243 159249 159253 159255 159259 159265 159271 159273 159279 159283 159285 159291 159295 159301 159309 203614
| 元素 | A | B | C |
| 结构信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3s104sx,有+1、+2两种常见化合价 |
(2)用氢键表示式写出A的氢化物溶液中存在的所有氢键N-H…N-N-H…O-O-H…N-O-H…O-;A的氢化物分子结合一个H+形成阳离子后,其键角变大(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为[Cu(NH3)4]SO4,
(4)科学家通过X射线推测胆矾中微粒间的作用力,胆矾的结构示意图
可简单表示如图1:

则胆矾晶体中含有ABCE
A.配位键 B.离子键 C.极性共价键 D.金属键 E.氢键F.非极性共价键
(5)下列分子结构图2中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.在以上分子中,中心原子采用sp3杂化形成化学键是①③④(填写序号).
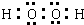 ;[Fe(C2O4)3]3-的名称是三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根).
;[Fe(C2O4)3]3-的名称是三草酸合铁(Ⅲ)离子(或三草酸合铁离子,或三草酸合铁酸根).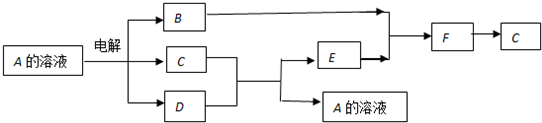
 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的核电荷数依次递增.B原子的P轨道半充满,形成氢化物的沸点是同主族元素的氢化物中最低的.D原子得到一个电子后3P轨道全充满.A+比D原子形成的离子少一个电子层.C与A形成A2C型离子化合物.E的原子序数为31,F与B属同一主族,E与F形成的化合物常用于制造半导体.根据以上信息,回答下列问题: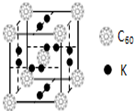 C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.
C60以其完美的球形结构受到科学家的高度重视,从此掀起了球形分子的研究热潮.继C60后,科学家又合成了Si60、N60等球形分子.