17.下面均是正丁烷与氧气反应的热化学方程式(25℃,101kPa):
①C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(l);△H=-2878KJ/mol
②C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(g);△H=-2658KJ/mol
③C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(l);△H=-1746KJ/mol
④C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(g);△H=-1526KJ/mol
由此判断,正丁烷的燃烧热是( )
①C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(l);△H=-2878KJ/mol
②C4H10(g)+$\frac{13}{2}$O2 (g)═4CO2(g)+5H2O(g);△H=-2658KJ/mol
③C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(l);△H=-1746KJ/mol
④C4H10(g)+$\frac{9}{2}$O2 (g)═4CO(g)+5H2O(g);△H=-1526KJ/mol
由此判断,正丁烷的燃烧热是( )
| A. | 2878KJ/mol | B. | 2658KJ/mol | C. | 1746KJ/mol | D. | 1526KJ/mol |
16.在pH=1的无色透明溶液中,能大量共存的离子组是( )
| A. | Al3+、Ag+、NO3-、Cl- | B. | K+、NH4+、NO3-、CO32- | ||
| C. | Fe3+、Ba2+、Cl-、NO3- | D. | Zn2+、Na+、NO3-、SO42- |
15.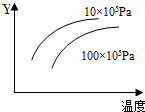 由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
 由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )
由可逆反应测绘出图象如下,纵坐标Y为生成物在平衡混合物中的体积百分含量,下列对该反应的判断正确的是( )| A. | 正反应为一定为放热反应 | B. | 逆反应为体积缩小的反应 | ||
| C. | 升高温度,平衡常数K值减小 | D. | 该反应在一定条件下可自发进行 |
14.根据反应式:2H2S+SO2=3S+2H2O,可判断氧化产物和还原产物的质量比( )
| A. | 24:9 | B. | 2:1 | C. | 1:2 | D. | 9:24 |
13.下列离子方程式正确的是( )
| A. | 硫酸溶液与氢氧化钡溶液混合:Ba2++SO42-=BaSO⒋↓ | |
| B. | 稀硫酸中加入铜片:Cu+2H+=Cu2++H2↑ | |
| C. | 氧化铜溶于盐酸:O2-+2H+=H2O | |
| D. | 二氧化碳通入足量澄清石灰水:Ca2++2OHˉ+CO2=CaCO3↓+H2O |
12.下列有关气体摩尔体积的描述中正确的是( )
| A. | 气体摩尔体积的数值是固定不变的,都约为22.4L | |
| B. | 通常情况的气体摩尔体积约为22.4L | |
| C. | 标准状况下的气体的摩尔体积约为22.4L | |
| D. | 标准状况下,气体的摩尔体积约为22.4L/mol |
10.写出下列物质的电离方程式:
KOHKOH═K++OH-
CuCl2CuCl2=Cu2++2Cl-
Fe2(SO4)3Fe2(SO4)3=2Fe3++3SO42-
Na2SNa2S=2Na++S2-.
KOHKOH═K++OH-
CuCl2CuCl2=Cu2++2Cl-
Fe2(SO4)3Fe2(SO4)3=2Fe3++3SO42-
Na2SNa2S=2Na++S2-.
9.下列变化中,一定要加入适当的还原剂才能实现的是( )
0 159107 159115 159121 159125 159131 159133 159137 159143 159145 159151 159157 159161 159163 159167 159173 159175 159181 159185 159187 159191 159193 159197 159199 159201 159202 159203 159205 159206 159207 159209 159211 159215 159217 159221 159223 159227 159233 159235 159241 159245 159247 159251 159257 159263 159265 159271 159275 159277 159283 159287 159293 159301 203614
| A. | Fe2O3-Fe | B. | H2-H2O | C. | KClO3-KCl | D. | CO2-CaCO3 |