4.一种烃的结构可表示为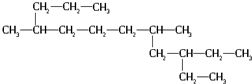 ,用系统命名法命名,该烃的名称为( )
,用系统命名法命名,该烃的名称为( )
 ,用系统命名法命名,该烃的名称为( )
,用系统命名法命名,该烃的名称为( )| A. | 4,8-二甲基-10-乙基12烷 | B. | 5,9-二甲基-3-乙基十二烷 | ||
| C. | 5-甲基-3-乙基-9-丙基十一烷 | D. | 3,9-二甲基-4-乙基十二烷 |
1.下列说法正确的是( )
0 159104 159112 159118 159122 159128 159130 159134 159140 159142 159148 159154 159158 159160 159164 159170 159172 159178 159182 159184 159188 159190 159194 159196 159198 159199 159200 159202 159203 159204 159206 159208 159212 159214 159218 159220 159224 159230 159232 159238 159242 159244 159248 159254 159260 159262 159268 159272 159274 159280 159284 159290 159298 203614
| A. | 按系统命名法,化合物 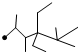 的名称是 2,3,5,5-四甲基-4,4-二乙基己烷 的名称是 2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 | |
| D. | 结构片段为 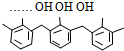 …的高聚物,其单体是甲醛和苯酚 …的高聚物,其单体是甲醛和苯酚 |
 2,3-二甲基戊烷,C7H16;
2,3-二甲基戊烷,C7H16; 2,3,3-三甲基戊烷,C8H18.
2,3,3-三甲基戊烷,C8H18. 的名称是2,5二甲基-3-乙基己烷.
的名称是2,5二甲基-3-乙基己烷.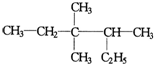 3,3,4-三甲基己烷
3,3,4-三甲基己烷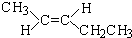 反-2-戊烯
反-2-戊烯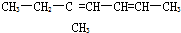 5-甲基-2,4一庚二烯
5-甲基-2,4一庚二烯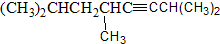 2,5,7-三甲基-3-辛炔.
2,5,7-三甲基-3-辛炔.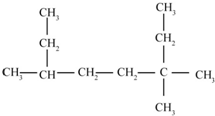 的名称为3,3,6-三甲基辛烷
的名称为3,3,6-三甲基辛烷 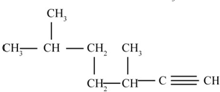 的名称为3,6-二甲基-1-庚炔
的名称为3,6-二甲基-1-庚炔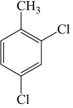 .
.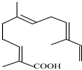 ,其分子式为C15H22O2.
,其分子式为C15H22O2.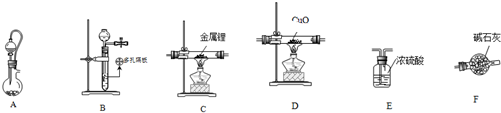
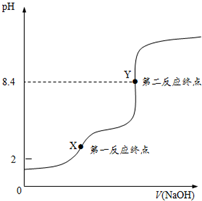 H2C2O4•2H2O(草酸,二元弱酸)和邻苯二甲酸氢钾均可作为标定NaOH溶液浓度的基准物质,从而获得NaOH标准溶液.
H2C2O4•2H2O(草酸,二元弱酸)和邻苯二甲酸氢钾均可作为标定NaOH溶液浓度的基准物质,从而获得NaOH标准溶液.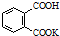 ,摩尔质量为204g•mol-1,易溶于水的固
,摩尔质量为204g•mol-1,易溶于水的固