7.下列说法正确的是( )


| A. | 按系统命名法命名,图1化合物的名称是2,4,6一三甲基-5-乙基庚烷 | |
| B. | 图2有机物的一种芳香族同分异构体能发生银镜反应 | |
| C. | 图2有机物能使酸性高锰酸钾溶液褪色 | |
| D. | 图3为髙分子化合物,其单体为对苯二甲酸和乙二醇 |
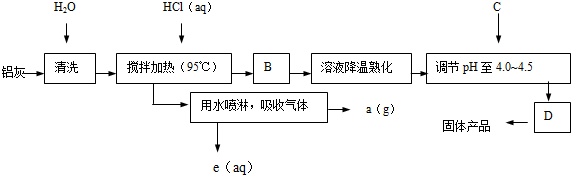
5.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌.
Ⅰ、制取氯化锌主要工艺如图:
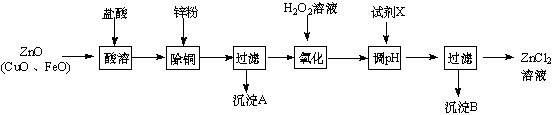
已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
(1)加入H2O2溶液发生反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)流程图中,为了降低溶液的酸度,试剂X可以是abc (选填序号:a.ZnO;b.Zn(OH)2;c.Zn2(OH)2CO3;d.ZnSO4);pH应调整到3.2≤pH<5.2.
(3)氯化锌能催化乳酸(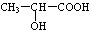 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为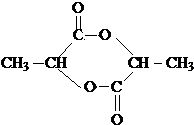 ,聚乳酸的结构简式为
,聚乳酸的结构简式为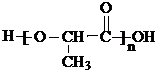 .
.
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)═Na2[Zn(OH)4](aq)},然后电解浸取液.
(4)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
Ⅰ、制取氯化锌主要工艺如图:

已知:Zn及化合物的性质与Al及化合物的性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.如表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)流程图中,为了降低溶液的酸度,试剂X可以是abc (选填序号:a.ZnO;b.Zn(OH)2;c.Zn2(OH)2CO3;d.ZnSO4);pH应调整到3.2≤pH<5.2.
(3)氯化锌能催化乳酸(
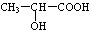 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ,聚乳酸的结构简式为
,聚乳酸的结构简式为 .
.Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)═Na2[Zn(OH)4](aq)},然后电解浸取液.
(4)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
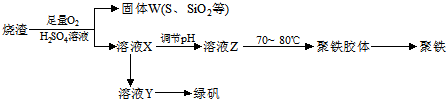
3.乙苯是一种用途广泛的有机原料,可制备多种化工产品.
(一)制备α-氯乙基苯的反应如下:
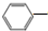 CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$
CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$ CHCl-CH3(g)+HCl(g)△H>0
CHCl-CH3(g)+HCl(g)△H>0
T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯摩尔分数随时间变化如下表所示:
(1)若初始投入乙苯为2mol,恒压容器容积10L,用氯气表示该反应0~5分钟内的速率υ(Cl2)=0.032mol/(L•min).T℃时,计算该反应的化学平衡常数K=16.6分钟时,仅改变一种条件破坏了平衡,则改变的外界条件为升高温度.
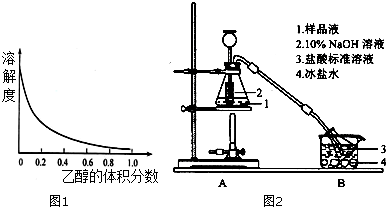
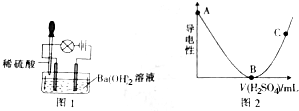
(2)图1中能正确反映平衡常数K随温度变化关系的曲线为b(填曲线标记字母),其判断理由是正反应为吸热反应,其他条件不变,温度升高K变大.
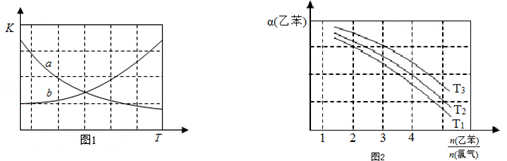
(3)乙苯的平衡转化率α(乙苯)随反应物投料比和温度的关系如图2所示,图2中的温度由大到小为T3>T2>T1,其判断理由是正反应为吸热反应,其他条件不变,温度升高,平衡正向移动,乙苯转化率增加.
(二)催化脱氢生产苯乙烯的反应如下:
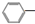 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)△H=+124kJ/mol
CH=CH2(g)+H2(g)△H=+124kJ/mol
(4)气相反应的化学平衡常数有多种表示方法,可用各气体摩尔分数代替浓度项表示平衡常数,写出上述反应的平衡常数表达式Kχ=$\frac{λ(氢气)λ(苯乙烯)}{λ(乙苯)}$.(用符号χ表示气体摩尔分数).
(5)工业上,在恒压条件下进行上述反应时,将乙苯与水蒸气的混合气体通入反应器中(已知水蒸气不参与反应),加入水蒸气可以使乙苯的转化率增大,用化学平衡理论解释乙苯转化率增加的原因恒压条件,加水蒸气体积增大,相当于减压,平衡向气体分子数增大的方向移动,即正向移动,乙苯转化率增加.
(一)制备α-氯乙基苯的反应如下:
 CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$
CH2CH3(g)+Cl2(g)$\stackrel{催化剂}{?}$ CHCl-CH3(g)+HCl(g)△H>0
CHCl-CH3(g)+HCl(g)△H>0T℃时,向一恒压密闭容器中充入等物质的量的乙苯气体和氯气发生上述反应(已排除其他反应干扰),测得乙苯摩尔分数随时间变化如下表所示:
| 时间/(min) | 0 | 2 | 5 | 6 | 9 | 10 |
| χ(乙苯) | 0.5 | 0.25 | 0.1 | 0.1 | 0.05 | 0.05 |
(2)图1中能正确反映平衡常数K随温度变化关系的曲线为b(填曲线标记字母),其判断理由是正反应为吸热反应,其他条件不变,温度升高K变大.

(3)乙苯的平衡转化率α(乙苯)随反应物投料比和温度的关系如图2所示,图2中的温度由大到小为T3>T2>T1,其判断理由是正反应为吸热反应,其他条件不变,温度升高,平衡正向移动,乙苯转化率增加.
(二)催化脱氢生产苯乙烯的反应如下:
 CH2CH3(g)$\stackrel{催化剂}{?}$
CH2CH3(g)$\stackrel{催化剂}{?}$ CH=CH2(g)+H2(g)△H=+124kJ/mol
CH=CH2(g)+H2(g)△H=+124kJ/mol(4)气相反应的化学平衡常数有多种表示方法,可用各气体摩尔分数代替浓度项表示平衡常数,写出上述反应的平衡常数表达式Kχ=$\frac{λ(氢气)λ(苯乙烯)}{λ(乙苯)}$.(用符号χ表示气体摩尔分数).
(5)工业上,在恒压条件下进行上述反应时,将乙苯与水蒸气的混合气体通入反应器中(已知水蒸气不参与反应),加入水蒸气可以使乙苯的转化率增大,用化学平衡理论解释乙苯转化率增加的原因恒压条件,加水蒸气体积增大,相当于减压,平衡向气体分子数增大的方向移动,即正向移动,乙苯转化率增加.
1.对水的电离平衡不产生影响的粒子是( )
| A. |  | B. | 26M3+ | C. | 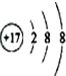 | D. | 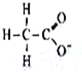 |
9.分子式为C8H18,一氯代物只有一种的烷烃的名称为( )
0 159102 159110 159116 159120 159126 159128 159132 159138 159140 159146 159152 159156 159158 159162 159168 159170 159176 159180 159182 159186 159188 159192 159194 159196 159197 159198 159200 159201 159202 159204 159206 159210 159212 159216 159218 159222 159228 159230 159236 159240 159242 159246 159252 159258 159260 159266 159270 159272 159278 159282 159288 159296 203614
| A. | 2,2,3,3-四甲基丁烷 | B. | 3,4-二甲基己烷 | ||
| C. | 2,2,3-三甲基戊烷 | D. | 3-甲基-3-乙基戊烷 |