6.原子的种类决定于原子的( )
| A. | 核电荷数 | B. | 最外层电子数 | ||
| C. | 核内质子数和中子数 | D. | 相对原子质量的大小 |
5.草酸二酯(CPPO)结构简式如图所示,下列有关草酸二酯的说法错误的是( )

| A. | 草酸二酯属于芳香族化合物 | |
| B. | 1mol草酸二酯最多可与4molNaOH反应 | |
| C. | 草酸二酯难溶于水 | |
| D. | 草酸二酯的分子式为C26H24O8Cl6 |
2.实验室现有两种酸碱指示剂,其pH变色范围如下:甲基橙:3.1~4.4;酚酞:8.2~10.0.用0.1000mol/L的稀硫酸滴定未知浓度的NaHCO3溶液,当反应恰好完全时,下列叙述正确的是( )
| A. | 可选用酚酞作指示剂,溶液由红色变为无色 | |
| B. | 可选用酚酞作指示剂,溶液由无色变为红色 | |
| C. | 可选用甲基橙作指示剂,溶液由黄色变为橙色 | |
| D. | 可选用甲基橙作指示剂,溶液由橙色变为红色 |
20.组成生命细胞的11种宏量元素(约占人体总质量的99.97%),全部位于周期表的前20号.其中组成人体蛋白质、脂肪、碳水化合物和核酸的主要有6种元素.
(1)这六种元素中除H、C、O、P、S外,应该还有N(写元素符号),它的原子最外层共有5种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置第二周期IVA族.CO2是一种温室气体,它的电子式为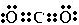 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
(2)糖类是人体获得能量的来源之一.已知1mol 葡萄糖在人体内完全氧化为二氧化碳和水,放出2804kJ的热量,该反应的热化学方程式C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804kJ•mol-1.
(3)元素周期表中元素的性质存在递变规律,下列关系正确的是D(填序号).
A、离子半径:S2->Na+>O2->H+ B、与水反应的剧烈程度:K>Na>Mg>Ca
C、熔点:CO2>SiO2>Na2O>SO3 D、还原性:PH3>H2S>HCl>HF
(4)下表为部分非金属元素与氢形成共价键的键长与键能数据:
根据表中数据,归纳共价键键能与键长的关系同类分子中(同主族元素原子与相同其他原子等合理均可),键长越小,键能越大..
(1)这六种元素中除H、C、O、P、S外,应该还有N(写元素符号),它的原子最外层共有5种不同运动状态的电子;与它同周期,且单质熔点最高的元素在周期表中的位置第二周期IVA族.CO2是一种温室气体,它的电子式为
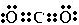 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.(2)糖类是人体获得能量的来源之一.已知1mol 葡萄糖在人体内完全氧化为二氧化碳和水,放出2804kJ的热量,该反应的热化学方程式C6H12O6(s)+6O2(g)→6CO2(g)+6H2O(l)△H=-2804kJ•mol-1.
(3)元素周期表中元素的性质存在递变规律,下列关系正确的是D(填序号).
A、离子半径:S2->Na+>O2->H+ B、与水反应的剧烈程度:K>Na>Mg>Ca
C、熔点:CO2>SiO2>Na2O>SO3 D、还原性:PH3>H2S>HCl>HF
(4)下表为部分非金属元素与氢形成共价键的键长与键能数据:
| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
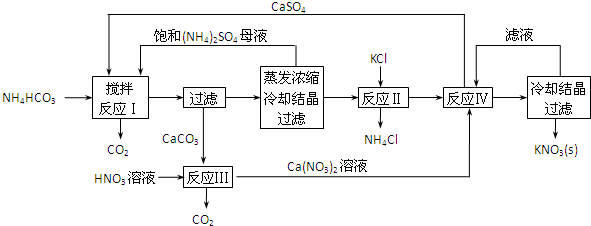
19.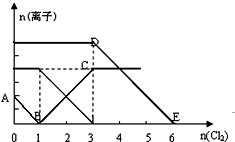 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )
 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如图所示.有关说法正确的是( )| A. | 线段BC代表Cl-数目的变化情况 | |
| B. | 原混合溶液中c(FeBr2)=6mol/L | |
| C. | 当通入Cl22mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2→2Fe3++I2+4 Cl- | |
| D. | 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
18.食品卫生与身体健康密切相关,下列物质可以用作食品添加剂的是( )
0 159079 159087 159093 159097 159103 159105 159109 159115 159117 159123 159129 159133 159135 159139 159145 159147 159153 159157 159159 159163 159165 159169 159171 159173 159174 159175 159177 159178 159179 159181 159183 159187 159189 159193 159195 159199 159205 159207 159213 159217 159219 159223 159229 159235 159237 159243 159247 159249 159255 159259 159265 159273 203614
| A. | 三聚氰胺 | B. | 苏丹红 | C. | 甲醇 | D. | 柠檬酸钠 |