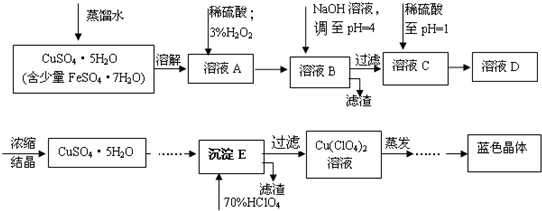
15.六水合高氯酸铜[Cu(C1O4)2•6H2O]是一种蓝色晶体,易溶于水,120℃时开始分解.实验室用硫酸铜的粗产品制备少量高氯酸铜晶体的流程如下:
已知:
(1)写出A→B过程中发生反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.
(2)溶液C中加入稀硫酸调至pH=1的目的是防止硫酸铜溶液在蒸发浓缩过程中Cu2+发生水解而得不到纯净的晶体.
(3)如欲检验溶液C中的杂质是否除净,其操作是取少量溶液,加入KSCN溶液(NH4SCN溶液),观察溶液是否仍然为蓝色.
(4)蒸发至有晶膜出现(填写现象),然后经过冷却结晶、过滤、洗涤、低温烘干(或自然干燥)(填写操作),得到纯净的蓝色晶体.
(5)为了测定硫酸铜的粗产品的纯度,某同学称量硫酸铜的粗产品2.000g、加水溶解、加入过量NaOH溶液、(填写实验步骤)过滤、洗涤沉淀、在空气中灼烧,至质量不再改变时,称得质量为0.6348g.
(6)该样品的纯度为91.9%.如果样品的实际纯度为93.2%,则测定的相对误差为-1.4%.

已知:
| 离子 | 溶液pH值 | |
| 开始沉淀 | 沉淀完全 | |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
(2)溶液C中加入稀硫酸调至pH=1的目的是防止硫酸铜溶液在蒸发浓缩过程中Cu2+发生水解而得不到纯净的晶体.
(3)如欲检验溶液C中的杂质是否除净,其操作是取少量溶液,加入KSCN溶液(NH4SCN溶液),观察溶液是否仍然为蓝色.
(4)蒸发至有晶膜出现(填写现象),然后经过冷却结晶、过滤、洗涤、低温烘干(或自然干燥)(填写操作),得到纯净的蓝色晶体.
(5)为了测定硫酸铜的粗产品的纯度,某同学称量硫酸铜的粗产品2.000g、加水溶解、加入过量NaOH溶液、(填写实验步骤)过滤、洗涤沉淀、在空气中灼烧,至质量不再改变时,称得质量为0.6348g.
(6)该样品的纯度为91.9%.如果样品的实际纯度为93.2%,则测定的相对误差为-1.4%.
13.下表为元素周期表的一部分.
(1)表中元素F的非金属性最强;元素K的金属性最强;元素Br的单质室温下呈液态(填写元素符号);
(2)表中元素 (11)的原子结构示意图是 ;
;
(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 四 | (11) | (12) | (13) | ||||
(2)表中元素 (11)的原子结构示意图是
 ;
;(3)表中元素⑥⑨⑩氢化物的稳定性顺序为HF>HCl>H2S(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:HClO4>H2SO4.
8.常温下,用 0.1000mol/L NaOH 溶液分别滴定 20.00mL 0.1000mol/L HCl 溶液和 20.00mL0.1000mol/L CH3COOH 溶液,得到2条滴定曲线,如图所示:
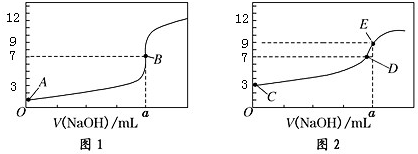
以下说法正确的是( )

以下说法正确的是( )
| A. | 图 1 是滴定 CH3COOH 溶液的曲线 | |
| B. | 图 2 若用甲基橙作指示剂达到滴定终点时,则溶液由黄色变为红色 | |
| C. | 点 D 所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 如果 C、E 两点对应的 pH 分别为 3、9,则水电离的氢离子浓度之比为 1:100 |
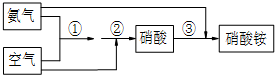
7.图1曲线a和b是盐酸与氢氧化钠的相互滴定的滴定曲线,下列叙述不正确的是( )

0 159078 159086 159092 159096 159102 159104 159108 159114 159116 159122 159128 159132 159134 159138 159144 159146 159152 159156 159158 159162 159164 159168 159170 159172 159173 159174 159176 159177 159178 159180 159182 159186 159188 159192 159194 159198 159204 159206 159212 159216 159218 159222 159228 159234 159236 159242 159246 159248 159254 159258 159264 159272 203614

| A. | 盐酸的物质的量浓度为1 mol•L-1,配制100 mL该溶液可用图3装置进行 | |
| B. | P点时反应恰好完全,溶液呈中性 | |
| C. | 曲线a是氢氧化钠溶液滴定盐酸的滴定曲线,可在图2的装置中进行 | |
| D. | 如果锥形瓶用待测液润洗,会使测定结果偏高 |
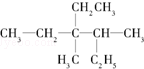 用系统命名法命名:3,4-二甲基-3-乙基己烷.
用系统命名法命名:3,4-二甲基-3-乙基己烷.
 .
. ,A与B可形成另一种气态化合物Z,写出实验室制取Z的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
,A与B可形成另一种气态化合物Z,写出实验室制取Z的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
 .
.