14.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如下:
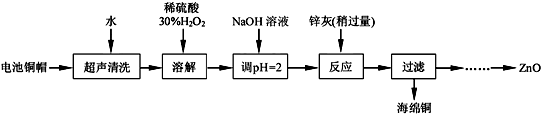
(1)①写出铜帽溶解过程中发生反应的化学方程式Cu+H2O2+H2SO4=CuSO4+2H2O.
②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 I2+2$S_2^{\;}O_3^{2-}$═2I-+$S_4^{\;}O_6^{2-}$
①滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为蓝色褪去并半分钟内不恢复.
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会偏高(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
由回收铜后的滤液制备ZnO的实验步骤依次为:
①向滤液中加入略过量30%的H2O2,使其充分反应;
②向反应后的溶液中滴加1.0moL•L-1的NaOH溶液,调节溶液的pH约为5(或3.2≤pH<5.9);
③过滤;
④向滤液中滴加1.0moL•L-1的氢氧化钠,调节pH约为10(或8.9≤pH≤11);
⑤过滤、洗涤、干燥
⑥900℃煅烧.

(1)①写出铜帽溶解过程中发生反应的化学方程式Cu+H2O2+H2SO4=CuSO4+2H2O.
②铜帽溶解后需将溶液中过量H2O2除去.除去H2O2的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:
2Cu2++4I-═2CuI(白色)↓+I2 I2+2$S_2^{\;}O_3^{2-}$═2I-+$S_4^{\;}O_6^{2-}$
①滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为蓝色褪去并半分钟内不恢复.
②若滴定前溶液中H2O2没有除尽,所测得的Cu2+的含量将会偏高(填“偏高”、“偏低”、“不变”).
(3)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算)
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
由回收铜后的滤液制备ZnO的实验步骤依次为:
①向滤液中加入略过量30%的H2O2,使其充分反应;
②向反应后的溶液中滴加1.0moL•L-1的NaOH溶液,调节溶液的pH约为5(或3.2≤pH<5.9);
③过滤;
④向滤液中滴加1.0moL•L-1的氢氧化钠,调节pH约为10(或8.9≤pH≤11);
⑤过滤、洗涤、干燥
⑥900℃煅烧.
12.有机物: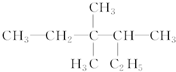 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 3,3二甲基4乙基戊烷 | B. | 3,3,4三甲基己烷 | ||
| C. | 2乙基3,3二甲基4乙基戊烷 | D. | 3,4,4三甲基己烷 |
10.下列热化学方程式书写正确的是(△H的绝对值均正确)( )
| A. | S+O2═2SO2;△H=-269kJ/mol(反应热) | |
| B. | 2NO2(g)═O2(g)+2NO(g);△H=+116.2kJ/mol(反应热) | |
| C. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0kJ/mol(燃烧热) | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热) |
9.25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是 393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
0 159076 159084 159090 159094 159100 159102 159106 159112 159114 159120 159126 159130 159132 159136 159142 159144 159150 159154 159156 159160 159162 159166 159168 159170 159171 159172 159174 159175 159176 159178 159180 159184 159186 159190 159192 159196 159202 159204 159210 159214 159216 159220 159226 159232 159234 159240 159244 159246 159252 159256 159262 159270 203614
| A. | C(s)+O2(g)═CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-890.3 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2 (g)+3H2O(l);△H=-1400 kJ/mol |
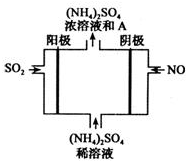 经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.
经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.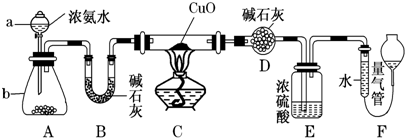

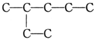
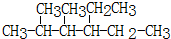 2,3-二甲基-3-乙基己烷
2,3-二甲基-3-乙基己烷 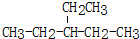 2-乙基戊烷
2-乙基戊烷 氮元素可形成卤化物、叠氮化物及络合物等.
氮元素可形成卤化物、叠氮化物及络合物等.