5. (1)已知A和B为第三周期元素,其原子的第一至第四电离能如表1所示:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表1所示:
表1
A通常显+3价,A的电负性>B的电负性(填“>”、“<”或“=”).
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据表2有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中的化学键C-C、C-N、C-S的键能大,紫外光的能量足以使这些键断裂,从而破坏蛋白质分子.
表2
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是sp2和sp3.
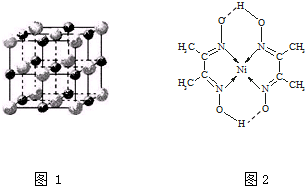
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),其中3种离子晶体的晶格能数据如表3:
表3
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:TiN>MgO>CaO>KCl.其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉
原料的是CrO2.
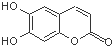
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键C.金属键 D.配位键E.氢键 F.非极性键
(6)温室效应主要由CO2引起,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2.若有1mol CH4生成,则有6molσ键和2molπ键断裂.
 (1)已知A和B为第三周期元素,其原子的第一至第四电离能如表1所示:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表1所示:表1
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)紫外光的光子所具有的能量约为399kJ•mol-1.根据表2有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中的化学键C-C、C-N、C-S的键能大,紫外光的能量足以使这些键断裂,从而破坏蛋白质分子.
表2
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),其中3种离子晶体的晶格能数据如表3:
表3
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能(kJ•mol-1) | 786 | 715 | 3401 |
(4)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉
原料的是CrO2.
(5)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键C.金属键 D.配位键E.氢键 F.非极性键
(6)温室效应主要由CO2引起,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2.若有1mol CH4生成,则有6molσ键和2molπ键断裂.
3. 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
 中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
中草药秦皮中含有的七叶树内酯,具有抗菌作用.若1mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )| A. | 2 mol Br2 2 mol NaOH | B. | 2 mol Br2 3 mol NaOH | ||
| C. | 3 mol Br2 4 mol NaOH | D. | 4 mol Br2 4 mol NaOH |
2.硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、水泥等,以下是工业利用硫酸钙的部分流程(图1):

(1)工业生产中产生的含SO2废气经石灰吸收和氧化后制成硫酸钙,写出反应方程式2SO2+2Ca(OH)2+O2=2CaSO4+2H2O.
(2)装置Ⅱ中,在一定条件下,二氧化硫和氧气发生反应时,温度与二氧化硫的转化率的关系如表所示:
①该反应的平衡常数表达式K=$\frac{c(SO{\;}_{3}){\;}^{2}}{c(SO{\;}_{2}){\;}^{2}c(O{\;}_{2})}$.
②关于此反应下列说法正确的是ac(填字母).
a.该反应△H<0
b.反应达到平衡时,SO2,O2,SO3 的浓度一定都相等
c.反应达到平衡状态时,v(SO2)正=2v(O2)逆
d.升高温度或使用催化剂都可提高SO2的转化率
③硫酸厂尾气(主要成分为SO2、O2和N2)中低浓度SO2的吸收有很多方法.用氨水吸收上述尾气,若尾气中
SO2与氨水恰好反应得到弱碱性的(NH4)2SO3溶液,则有关该溶液的下列关系正确的是ac (填字母).
a.c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
b.c(NH4+)+c (H+)=c (SO32-)+c (HSO3-)+c (OH-)
c.c(NH4+)>c (SO32-)>c (OH-)>c (H+)
(3)装置Ⅲ中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).
已知:①2CO(g)+O2(g)═2CO2(g)△H=-283kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
③2CH3OH(l)+3O2(g)═2CO2(g)+4H2O (l)△H=-725.8kJ•mol-1
试写出CO与H2在一定条件下反应生成CH3OH(l)的热化学方程式CO(g)+2H2(g)=CH3OH(l)△H=-350.2kJ•mol-1.
(4)在固态金属氧化物电解池中,一定条件下H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图2所示.
①Y端是电源的正极(填正极或负极).
②阴极的电极反应式为 CO2+2eˉ=CO+O2ˉ和H2O+2e-═H2↑+O2-.

(1)工业生产中产生的含SO2废气经石灰吸收和氧化后制成硫酸钙,写出反应方程式2SO2+2Ca(OH)2+O2=2CaSO4+2H2O.
(2)装置Ⅱ中,在一定条件下,二氧化硫和氧气发生反应时,温度与二氧化硫的转化率的关系如表所示:
| 温度/℃ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
②关于此反应下列说法正确的是ac(填字母).
a.该反应△H<0
b.反应达到平衡时,SO2,O2,SO3 的浓度一定都相等
c.反应达到平衡状态时,v(SO2)正=2v(O2)逆
d.升高温度或使用催化剂都可提高SO2的转化率
③硫酸厂尾气(主要成分为SO2、O2和N2)中低浓度SO2的吸收有很多方法.用氨水吸收上述尾气,若尾气中
SO2与氨水恰好反应得到弱碱性的(NH4)2SO3溶液,则有关该溶液的下列关系正确的是ac (填字母).
a.c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
b.c(NH4+)+c (H+)=c (SO32-)+c (HSO3-)+c (OH-)
c.c(NH4+)>c (SO32-)>c (OH-)>c (H+)
(3)装置Ⅲ中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO).
已知:①2CO(g)+O2(g)═2CO2(g)△H=-283kJ•mol-1
②2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
③2CH3OH(l)+3O2(g)═2CO2(g)+4H2O (l)△H=-725.8kJ•mol-1
试写出CO与H2在一定条件下反应生成CH3OH(l)的热化学方程式CO(g)+2H2(g)=CH3OH(l)△H=-350.2kJ•mol-1.
(4)在固态金属氧化物电解池中,一定条件下H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图2所示.
①Y端是电源的正极(填正极或负极).
②阴极的电极反应式为 CO2+2eˉ=CO+O2ˉ和H2O+2e-═H2↑+O2-.
1.已知H-H、H-O和O═O键的键能分别为436kJ•mol-1,463kJ•mol-1,495kJ•mol-1,下列热化学方程式正确的是( )
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-485 kJ•mol-1 | B. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=485 kJ•mol-1 | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=485 kJ•mol-1 | D. | 2H2(g)+O2(g)═2H2O(g)△H=-485 kJ•mol-1 |
13.下列反应中,氧化产物和还原产物的物质的量之比为1:1的是( )
| A. | 3NO2+H2═2HNO3+NO | B. | 4FeS2+11O2$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8SO2 | ||
| C. | 3Cl2+8NH3═N2+6NH4Cl | D. | 2Na+2NH3(液)═2NaNH2+H2 |
12.为了提高氮水中次氯酸的浓度,增强氯水的漂白力,可向氯水中加入的试剂是( )
0 159075 159083 159089 159093 159099 159101 159105 159111 159113 159119 159125 159129 159131 159135 159141 159143 159149 159153 159155 159159 159161 159165 159167 159169 159170 159171 159173 159174 159175 159177 159179 159183 159185 159189 159191 159195 159201 159203 159209 159213 159215 159219 159225 159231 159233 159239 159243 159245 159251 159255 159261 159269 203614
| A. | CaCO3 | B. | Na2SO3 | C. | H2SO4 | D. | Ca(OH)2 |
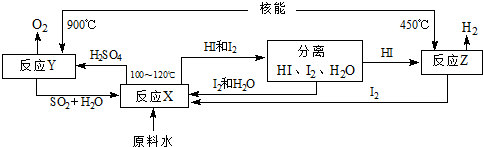
 +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$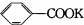 +2MnO2↓+1H2O+(1)KOH
+2MnO2↓+1H2O+(1)KOH 与C按1:1生成高分子化合物的反应方程式为
与C按1:1生成高分子化合物的反应方程式为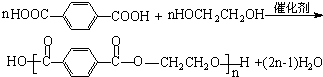 .
.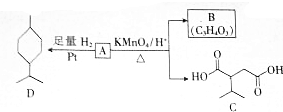
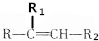 $→_{△}^{KMnO_{4}/H+}$
$→_{△}^{KMnO_{4}/H+}$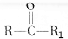 +R2COOH
+R2COOH .A与等物质的量的溴单质反应的产物有3种.
.A与等物质的量的溴单质反应的产物有3种. .
.