7. 某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )
某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )
 某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )
某分子的球棍模型如图所示.已知分子中所有原子的最外层均达到 8 电子稳定结构,原子间以单键相连.下列有关说法中一定错误的是( )| A. | X原子可能为第VA族元素 | |
| B. | 该分子中既含有极性共价键又含有非极性共价键 | |
| C. | Y 原子可能为第ⅠA 族或第ⅦA 族元素元素 | |
| D. | 从圆球的大小分析,该分子可能为 N2F4 |
6.在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g)?C(g)+D(g)已达到平衡状态( )
①混合气体的压强
②混合气体的密度
③各气体物质的物质的量浓度
④气体的总物质的量
⑤混合气体的平均相对分子质量
⑥A 的质量.
①混合气体的压强
②混合气体的密度
③各气体物质的物质的量浓度
④气体的总物质的量
⑤混合气体的平均相对分子质量
⑥A 的质量.
| A. | ①②③⑥ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ①③⑤⑥ |
5.少量铁片与 l00mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加 H2O
②加 KNO3溶液
③滴入几滴浓盐酸
④加入少量铁粉
⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
⑧改用 10mL 0.1mol/L 盐酸.
①加 H2O
②加 KNO3溶液
③滴入几滴浓盐酸
④加入少量铁粉
⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液
⑦升高温度(不考虑盐酸挥发)
⑧改用 10mL 0.1mol/L 盐酸.
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ③⑥⑦⑧ |
4.主链含5个碳原子,有甲基、乙基 2 个支链的烷烃有( )
| A. | 2 种 | B. | 3 种 | C. | 4 种 | D. | 5 种 |
3.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 1molCl2 与过量乙烷在光照下反应,生成的有机物中含有氯原子的总数为2NA | |
| B. | 1molC3H8 中含有的共用电子对数为11NA | |
| C. | 1.5g 甲基含有的质子数和电子数之和为1.8NA | |
| D. | 标况下,11.2 L癸烷含有的原子个数为16 NA |
1.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下.

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、A13+、Ca2+和Mg2+.
(1)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(2)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.滤液II中阳离子主要有Na+、Mg2+、Ca2+;
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液II中的金属阳离子是Ca2+、Mg2+.
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.
0 159070 159078 159084 159088 159094 159096 159100 159106 159108 159114 159120 159124 159126 159130 159136 159138 159144 159148 159150 159154 159156 159160 159162 159164 159165 159166 159168 159169 159170 159172 159174 159178 159180 159184 159186 159190 159196 159198 159204 159208 159210 159214 159220 159226 159228 159234 159238 159240 159246 159250 159256 159264 203614

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、A13+、Ca2+和Mg2+.
(1)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(2)H2O2的作用是将滤液I中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | - | - | - |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
(4)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液II中的金属阳离子是Ca2+、Mg2+.
(5)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.
 氮是重要的非金属元素,其单质用途之一是制取氨气,反应方程式为:N2(g)+3H2(g)?2NH3(g):回答下列问题:
氮是重要的非金属元素,其单质用途之一是制取氨气,反应方程式为:N2(g)+3H2(g)?2NH3(g):回答下列问题: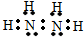 .
.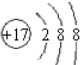 ;
;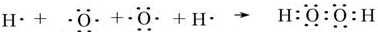 ;
;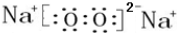 ,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,lmolH发生该反应转移电子数为6.02×1023或NA;
,该化合物和B与D形成的某化合物反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,lmolH发生该反应转移电子数为6.02×1023或NA;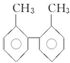
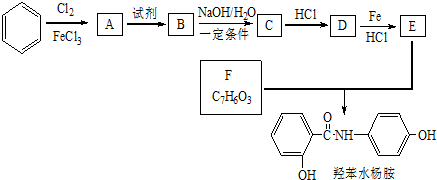
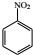 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$
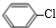 +HNO3$→_{△}^{浓H_{2}SO_{4}}$
+HNO3$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.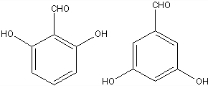 、
、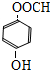 .
.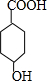 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$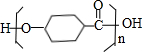 +(n-1)H2O.
+(n-1)H2O.