19.下列说不正确的是( )
| A. | CH3CH(CH3)CH(CH3)2的系统名称是2,3一二甲基丁烷 | |
| B. | 石油化工中裂化是为了提高轻质油的产量和质量 | |
| C. | 维勒在制备氰酸铰时得到了尿素,打破了“生命力论”的统治地位 | |
| D. | 乙醇和浓硫酸加热到170°时发生脱水生成乙醚 |
17.下列说法正确的是( )
| A. | 存在 2,2-二甲基-3-戊炔 | |
| B. | 月桂烯分子中(  )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | CF2Cl2存在两种同分异构体 | |
| D. | 用红外光谱法可鉴别二甲醚和乙醇 |
16.下列有机物命名正确的是( )
0 159055 159063 159069 159073 159079 159081 159085 159091 159093 159099 159105 159109 159111 159115 159121 159123 159129 159133 159135 159139 159141 159145 159147 159149 159150 159151 159153 159154 159155 159157 159159 159163 159165 159169 159171 159175 159181 159183 159189 159193 159195 159199 159205 159211 159213 159219 159223 159225 159231 159235 159241 159249 203614
| A. | 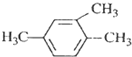 1,3,4-三甲苯 1,3,4-三甲苯 | B. | 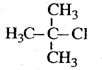 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | ||
| C. | 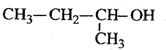 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. | 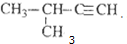 2-甲基-3-丁炔 2-甲基-3-丁炔 |
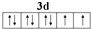 ,写出A、B形成化合物的电子式
,写出A、B形成化合物的电子式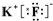
 的烃可命名为:2,4-二甲基-3-乙基戊烷.
的烃可命名为:2,4-二甲基-3-乙基戊烷.