9.下列物质的化学名称分别是:Na2S2O3叫硫代硫酸钠;CaSx 叫多硫化钙;BaO2叫过氧化钡.根据上述命名规律,K2CS3应读作( )
| A. | 三硫代碳酸钾 | B. | 多硫碳化钾 | C. | 过硫碳酸钾 | D. | 超硫碳酸钾 |
8.现有液化石油气、天然气、氢气三种物质,根据它们的某种性质可以归为一类.下列跟上述三种物质属于一类物质的是( )
| A. | CO2 | B. | N2 | C. | SO2 | D. | CO |
7.过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等.某化学兴趣小组取一定量的过氧化氢溶液,探究了过氧化氢的性质,并准确测定了过氧化氢的含量.
Ⅰ.探究过氧化氢的性质
(1)该化学小组设计了两个实验,分别证明了H2O2的两个性质.请将他们的实验现象和验证性质填入下表:
(2)常温下,向H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是ACD
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe2+和Fe3+的总量发生变化
D.H2O2生产过程要严格避免混入Fe2+
Ⅱ.测定过氧化氢的含量
(1)量取10.00mL密度为ρ g/mL的过氧化氢溶液,溶解后将溶液转移至250mL容量瓶(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.□MnO4-+□H2O2+□H+=□Mn2++□H2O+□□
该反应体现了H2O2的还原性.
(3)滴定时,将高锰酸钾标准溶液注入酸式 (填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色.
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”或“偏低”或“不变”).
Ⅰ.探究过氧化氢的性质
(1)该化学小组设计了两个实验,分别证明了H2O2的两个性质.请将他们的实验现象和验证性质填入下表:
| 实验所用试剂或操作 | 实 验 现 象 | 验证的性质 |
| 碘化钾淀粉溶液 | ||
| 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验. |
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是ACD
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe2+和Fe3+的总量发生变化
D.H2O2生产过程要严格避免混入Fe2+
Ⅱ.测定过氧化氢的含量
(1)量取10.00mL密度为ρ g/mL的过氧化氢溶液,溶解后将溶液转移至250mL容量瓶(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.□MnO4-+□H2O2+□H+=□Mn2++□H2O+□□
该反应体现了H2O2的还原性.
(3)滴定时,将高锰酸钾标准溶液注入酸式 (填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色.
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”或“偏低”或“不变”).
5.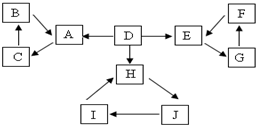 A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:
A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:
用化学用语回答下列问题:
(1)A、E、H中原子序数最大的元素的元素符号S,A、B、C共同含有的元素在周期表中的位置第三周期第IIIA族;
(2)指出H中化学键类型离子键和共价键,写出与H相对分子质量相同,且它们的阴离子所含的电子数、电荷数也均相同的化合物的电子式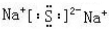 .
.
(3)常温下C溶液的PH<7,(填“<”、“>”或“=”)写出C溶液中通入少量盐酸生成B的化学方程式HCl+NaAlO2+H2O=Al(OH)3↓+NaCl.写出C溶液中滴加NaHCO3溶液的离子方程式AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-.
(4)Zn和Cu分别和一定量F的浓溶液反应,若产生的气体体积相等(相同条件下),则下列判断正确的是BD
A.产生的气体种类一定相同 B.转移的电子一定相同
C.消耗F的物质的量一定相同 D.消耗两种金属物质的量一定相同
(5)电解饱和J溶液产物之一为Y2,将一定量的Y2通入一定浓度的苛性钾溶液中,两者恰好完全反应,生成三种含Y元素的离子,其中YO3-、YO-两种离子物质的量之比为1:2,该反应的离子方程式是10OH-+5Cl2=2ClO-+ClO3-+7Cl-+5 H2O.
 A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:
A、B、C、D、E、F、G、H、I、J有如图所示的转化关系.图中所有物质均由短周期元素组成,且每个小三角形内的三种物质均至少含有第三周期中的一种相同元素.其它信息见表:| 编号 | 信息 | 编号 | 信息 |
| 1 | D为地壳中含量最高的元素组成的单质 | 4 | H为淡黄色固体化合物 |
| 2 | E为酸性气态氧化物 | 5 | 电解饱和J溶液是工业重要反应 |
| 3 | F的浓溶液常做干燥剂 | 6 | C为离子化合物,阴、阳离子均含金属元素 |
(1)A、E、H中原子序数最大的元素的元素符号S,A、B、C共同含有的元素在周期表中的位置第三周期第IIIA族;
(2)指出H中化学键类型离子键和共价键,写出与H相对分子质量相同,且它们的阴离子所含的电子数、电荷数也均相同的化合物的电子式
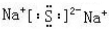 .
.(3)常温下C溶液的PH<7,(填“<”、“>”或“=”)写出C溶液中通入少量盐酸生成B的化学方程式HCl+NaAlO2+H2O=Al(OH)3↓+NaCl.写出C溶液中滴加NaHCO3溶液的离子方程式AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-.
(4)Zn和Cu分别和一定量F的浓溶液反应,若产生的气体体积相等(相同条件下),则下列判断正确的是BD
A.产生的气体种类一定相同 B.转移的电子一定相同
C.消耗F的物质的量一定相同 D.消耗两种金属物质的量一定相同
(5)电解饱和J溶液产物之一为Y2,将一定量的Y2通入一定浓度的苛性钾溶液中,两者恰好完全反应,生成三种含Y元素的离子,其中YO3-、YO-两种离子物质的量之比为1:2,该反应的离子方程式是10OH-+5Cl2=2ClO-+ClO3-+7Cl-+5 H2O.
2.以下物质中,可以一次将乙醇、乙酸、苯、四氯化碳四种物质都鉴别出来的是( )
0 159037 159045 159051 159055 159061 159063 159067 159073 159075 159081 159087 159091 159093 159097 159103 159105 159111 159115 159117 159121 159123 159127 159129 159131 159132 159133 159135 159136 159137 159139 159141 159145 159147 159151 159153 159157 159163 159165 159171 159175 159177 159181 159187 159193 159195 159201 159205 159207 159213 159217 159223 159231 203614
| A. | 金属钠 | B. | 溴水 | C. | 碳酸钠溶液 | D. | 酚酞试剂 |
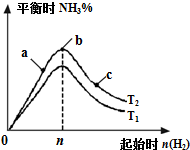 某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量):
某科研小组研究在其他条件不变的情况下,改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol 反应的影响,实验结果可表示成如图所示的规律(T表示温度,n表示物质的量): 如图所示装置:
如图所示装置: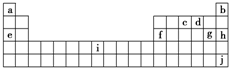
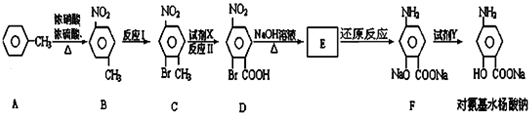
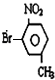 或
或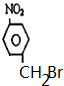 .
.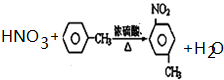 (注明反应条件).
(注明反应条件).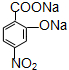 .
.