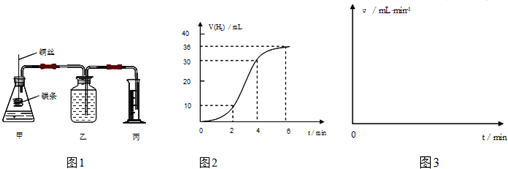
16.下列有关实验操作错误的是( )
| A. | 用药匙取用粉末状或小颗粒状固体 | B. | 用胶头滴管滴加少量液体 | ||
| C. | 给盛有$\frac{2}{3}$体积液体的试管加热 | D. | 倾倒液体时试剂瓶标签面向手心 |
15.用NA表示阿伏加德常数,以下的说法正确的是( )
| A. | 精炼铜时,阳极有1mol物质放电,阴极一定生成NA个铜原子 | |
| B. | 在标准状况下,NA个SO3 分子的质量是80g,其体积就为80/ρ (ρ为SO3的密度) | |
| C. | 1molNaHSO4 熔融液中,其阴阳离子总数目为3NA | |
| D. | PH=1的盐酸溶液中,H+的数目为0.1NA |
14.铁铜单质及其化合物的应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:
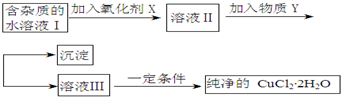
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
请回答下列问题:
(1)下列最适合作氧化剂X的是C
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入的物质Y是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3]如果不用物质Y而直接用可溶性碱溶液不能 (填“能”或者“不能”)达到目的.若不能,试解释原因加碱使Fe3+沉淀的同时也能使Cu2+沉淀(若填“能”,此空不用回答)
(3)最后不能(填“能”或者“不能”)直接蒸发得到CuCl2•2H2O?若不能,应该如何操作才能得到CuCl2•2H2O应在HCl气流中加热蒸发结晶(若填“能”,此空不用回答)
(4)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀
(5)若向溶液Ⅱ中加入镁粉,产生的气体是氢气,试解释原因镁粉与氯化铁、氯化铜水解生成的氢离子反应生成氢气.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(1)下列最适合作氧化剂X的是C
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入的物质Y是CuO[或Cu(OH)2、CuCO3、Cu2(OH)2CO3]如果不用物质Y而直接用可溶性碱溶液不能 (填“能”或者“不能”)达到目的.若不能,试解释原因加碱使Fe3+沉淀的同时也能使Cu2+沉淀(若填“能”,此空不用回答)
(3)最后不能(填“能”或者“不能”)直接蒸发得到CuCl2•2H2O?若不能,应该如何操作才能得到CuCl2•2H2O应在HCl气流中加热蒸发结晶(若填“能”,此空不用回答)
(4)若向溶液Ⅱ中加入碳酸钙,产生的现象是碳酸钙溶解,产生气泡和红褐色沉淀
(5)若向溶液Ⅱ中加入镁粉,产生的气体是氢气,试解释原因镁粉与氯化铁、氯化铜水解生成的氢离子反应生成氢气.
13.25℃时,下列有关溶液中微粒的物质的量浓度关系正确( )
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c (OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
12.下列说法中,不正确的是( )
| A. | 电解饱和食盐水或熔融氯化钠时,阳极的电极反应式均为2Cl--2e-═Cl2↑ | |
| B. | 钢铁发生吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-═Fe2+ | |
| C. | 精炼铜和电镀铜时,与电源负极相连的电极反应式均为Cu2++2e-═Cu | |
| D. | 酸性介质或碱性介质的氢氧燃料电池的正极反应式均为O2+2H2O+4e-═4OH- |
11.用CH4催化还原NOx,可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1 160kJ•mol-1
下列说法正确的是( )
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1 160kJ•mol-1
下列说法正确的是( )
| A. | 当反应相同体积的CH4时反应①②转移的电子数相同 | |
| B. | 由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H>-574 kJ•mol-1 | |
| C. | 反应②中当生成4.48 L CO2时转移的电子总数为1.60 mol | |
| D. | 若用标准状况下4.48 L CH4还原NO2生成N2和水蒸气,放出的热量为173.4 kJ |
10.下列说法正确的是( )
| A. | 化学反应一定伴随有热量的变化 | |
| B. | 活化能越大的化学反应其反应热数值也越大 | |
| C. | 反应热的产生是由于生成物与反应物的总能量不同 | |
| D. | 放热反应是由于反应物键能总和大于生成物键能总和 |
8.将密度为1.2g/cm3的盐酸溶液逐滴滴入到AgNO3溶液中,直到沉淀恰好完全为止,溶液的质量保持不变,则盐酸物质的量浓度为( )
| A. | 25.4% | B. | 50.8% | C. | 6mol/L | D. | 8.36mol/L |
7.下列有关NA叙述正确的是( )
0 158996 159004 159010 159014 159020 159022 159026 159032 159034 159040 159046 159050 159052 159056 159062 159064 159070 159074 159076 159080 159082 159086 159088 159090 159091 159092 159094 159095 159096 159098 159100 159104 159106 159110 159112 159116 159122 159124 159130 159134 159136 159140 159146 159152 159154 159160 159164 159166 159172 159176 159182 159190 203614
| A. | 标准状况下,1molSO3的气体体积为22.4L | |
| B. | 1mol铁粉与过量Cl2反应时,转移电子数为2NA | |
| C. | 含有2NA个氧原子的D2O质量为40g | |
| D. | 16gO2分子中含有的氧原子数为0.5NA |