7.下列各组物质互为同分异构体的是( )
| A. | O2和O3 | B. | CH3CH2CH2CH3和 | C. | 12C和13C | D. | CH4和CH3CH3 |
6.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 12 g C-13含有的原子数为NA个 | |
| B. | 46g NO2和46g N2O4含有的原子数均为3NA | |
| C. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| D. | 标准状况下,2.24L乙醇所含分子数为0.1 NA |
5.下列叙述正确的是( )
| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 | |
| B. | 用惰性电极精炼铜时,电解质溶液没有变化 | |
| C. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
4.下列的描述中不正确的是( )
| A. | 常温下,pH=1的醋酸溶液中,醋酸分子的数目一定大于0.1mol | |
| B. | 一定条件下的可逆反应,反应物的转化率不可能达到100% | |
| C. | 沉淀溶解转换的实质是沉淀溶解平衡的移动,平衡一般向生成更难溶物质的方向移动 | |
| D. | △H<0,△S>0的反应一定是自发进行的化学反应 |
3.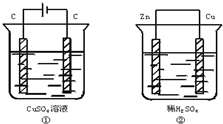 如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )
 如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )
如图两个装置中,溶液体积均为200mL,开始时电解质溶液的浓度均为0.1mol•L-1,工作一段时间后,测得导线上通过0.02mol电子,若不考虑盐水解和溶液体积的变化,则下列叙述正确的是( )| A. | 产生气体的体积:①>② | |
| B. | 电极总质量的变化:①增加,②减小 | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | 电极反应式:①装置中的阳极:4OH--4e-→2H2O+O2↑ ②装置中的负极:2H++2e-→H2↑ |
18.下列化学用语完全正确的一组是( )
0 158976 158984 158990 158994 159000 159002 159006 159012 159014 159020 159026 159030 159032 159036 159042 159044 159050 159054 159056 159060 159062 159066 159068 159070 159071 159072 159074 159075 159076 159078 159080 159084 159086 159090 159092 159096 159102 159104 159110 159114 159116 159120 159126 159132 159134 159140 159144 159146 159152 159156 159162 159170 203614
| A. | 电子式:次氯酸: ;过氧化钠: ;过氧化钠: ;羟基: ;羟基: | |
| B. | KHSO4熔融电离:KHSO4=K++H++SO42-;KHCO3溶解于水:KHCO3=K++H++CO32- | |
| C. | 高聚物化学式:聚异戊二烯: ;PVC: ;PVC: ;PE: ;PE: | |
| D. | 下列分子式代表的有机物均有可能与NaHCO3反应放出CO2:C5H12O2、C2H4O2、C7H8O |
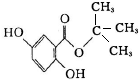
 龙胆酸甲酯是制取抗心律失常药物--氟卡尼的中间体.
龙胆酸甲酯是制取抗心律失常药物--氟卡尼的中间体.