17.将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.9mol,这些气体恰好能被500mL 2mol/L NaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为( )
| A. | 0.2 mol | B. | 0.4 mol | C. | 0.8 mol | D. | 0.9 mol |
16.某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究.
【查阅资料】25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
【实验探究】向2支均盛有1mL0.1mol/L的MgCl2溶液中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀;(1)分别向两支试管中加入不同试剂,记录实验现象如表:
(2)测得试管Ⅰ中所得混合溶液pH=6,则溶液中c(Fe3+)=4×10-14mol/L.
(3)同学们猜想实验Ⅱ中沉淀溶解的原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动.
猜想2:NH4Cl水解出来的H+与Mg(OH)2电离出OH-结合成水,使Mg(OH)2的溶解平衡正向移动.
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解.
①实验证明猜想正确的是1(填“1“或“2“).
②验证猜想时,设计实验向氢氧化镁沉淀中加NH4Cl和氨水混合液的理由是做对比分析,pH=8的NH4Cl和氨水混合液中c(H+)很小,可以否定猜想2.
【查阅资料】25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
【实验探究】向2支均盛有1mL0.1mol/L的MgCl2溶液中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀;(1)分别向两支试管中加入不同试剂,记录实验现象如表:
| 实验编号 | 加入试剂 | 实验现象 |
| Ⅰ | 2滴 0.1mol/L FeCl3 溶液 | ①白色沉淀转化为红褐色沉淀 |
| Ⅱ | 4mL2mol/LNH4Cl溶液 | ②白色沉淀溶解,得无色溶液 |
(3)同学们猜想实验Ⅱ中沉淀溶解的原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动.
猜想2:NH4Cl水解出来的H+与Mg(OH)2电离出OH-结合成水,使Mg(OH)2的溶解平衡正向移动.
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解.
①实验证明猜想正确的是1(填“1“或“2“).
②验证猜想时,设计实验向氢氧化镁沉淀中加NH4Cl和氨水混合液的理由是做对比分析,pH=8的NH4Cl和氨水混合液中c(H+)很小,可以否定猜想2.
15.下列说法不正确的是( )
| A. | “臭氧空洞”“温室效应”“光化学烟雾”“硝酸型酸雨”的形成过程都与氮氧化合物有关 | |
| B. | 石油裂解、煤的气化、海水制镁、石油中提取石蜡等过程中都包含化学变化 | |
| C. | 低碳经济就是以低耗能、低污染、低排放为基础的经济发展模式 | |
| D. | 可利用丁达尔效应鉴别氢氧化铁胶体和氯化铁溶液 |
12. 已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0
已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0
(1)SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H1=akJ/mol
SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H2=bkJ/mol
比较a<b(填<、>、=).
(2)反应速率v与反应物浓度的关系可用实验方法测定,v=k•cm(SO2)•cn (Cl2),k为反应速率常数.根据下述实验结果,求m=1n=1.
(3)恒温下,若在容积固定的2L密闭容器中,充入SO2、Cl2各2mol,发生可逆反应:SO2+Cl2?SO2Cl2,达到平衡时,以SO2的浓度改变表示反应速率v正、v逆与时间的关系如图,其中S表示面积,则SO2的平衡浓度为C.
A.1-S(bod) B.S(bod) C.1-S(aob) D.S(aob)
(4)若在催化剂作用下,将n molSO2与n molCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P,起始气体总体积为10L,t min时反应达到平衡,此时气体总体积为8L.
①此温度下,该反应的平衡常数Kp=$\frac{16}{9P}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器达平衡状态时,混合物中SO2Cl2的物质的量是0.2n.
(5)SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
已知25℃,Ksp(AgCl)=1.8×10-10,Ksp(Ag2SO4)=1.4×10-5,向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是Cl-,当第二种离子开始沉淀时,溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$=2.3×10-15.
 已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0
已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0(1)SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H1=akJ/mol
SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H2=bkJ/mol
比较a<b(填<、>、=).
(2)反应速率v与反应物浓度的关系可用实验方法测定,v=k•cm(SO2)•cn (Cl2),k为反应速率常数.根据下述实验结果,求m=1n=1.
| c(SO2)/mol•L-1 | c(Cl2)/mol•L-1 | v/mol•L-1•S-1 |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 8.0k |
A.1-S(bod) B.S(bod) C.1-S(aob) D.S(aob)
(4)若在催化剂作用下,将n molSO2与n molCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P,起始气体总体积为10L,t min时反应达到平衡,此时气体总体积为8L.
①此温度下,该反应的平衡常数Kp=$\frac{16}{9P}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器达平衡状态时,混合物中SO2Cl2的物质的量是0.2n.
(5)SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
已知25℃,Ksp(AgCl)=1.8×10-10,Ksp(Ag2SO4)=1.4×10-5,向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是Cl-,当第二种离子开始沉淀时,溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$=2.3×10-15.
10.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质).
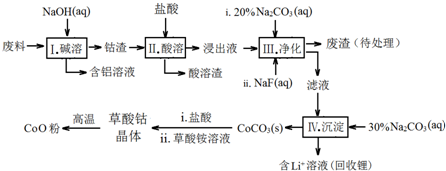
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应调节溶液的pH范围是3.2-7.15;废渣中的主要成分为Fe(OH)3、LiF.
(4)步骤Ⅲ中NaF参与的反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,[M (CoC2O4•2H2O)=183g/mol]受热过程中不同温度范围内分别得到一种固体物质,其质量如表.
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是3CoC2O4+2O2 $\frac{\underline{\;210℃-290℃\;}}{\;}$Co3O4+6CO2.
0 158959 158967 158973 158977 158983 158985 158989 158995 158997 159003 159009 159013 159015 159019 159025 159027 159033 159037 159039 159043 159045 159049 159051 159053 159054 159055 159057 159058 159059 159061 159063 159067 159069 159073 159075 159079 159085 159087 159093 159097 159099 159103 159109 159115 159117 159123 159127 159129 159135 159139 159145 159153 203614

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
(2)步骤Ⅱ中Co2O3与盐酸反应的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O.
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应调节溶液的pH范围是3.2-7.15;废渣中的主要成分为Fe(OH)3、LiF.
(4)步骤Ⅲ中NaF参与的反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀.
(5)在空气中加热5.49g草酸钴晶体(CoC2O4•2H2O)样品,[M (CoC2O4•2H2O)=183g/mol]受热过程中不同温度范围内分别得到一种固体物质,其质量如表.
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
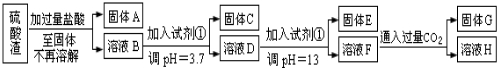
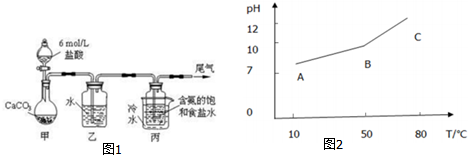
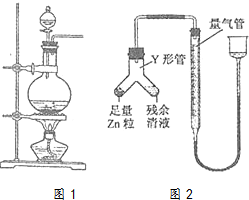 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示)
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示)