12.(1)下面不是污水处理方法的是A(填字母)A.过滤法 B.混凝法 C.中和法 D.沉淀法天然水中含有细菌,其主要成分是蛋白质,家庭中能杀灭水中细菌的简单方法:①添加合适的消毒剂、②加热或紫外线消毒等;
(2)现有一杯具有永久硬度的水,其中主要含有MgCl2、CaCl2.利用下列试剂中的一部分或全部,设计软化该水的实验方案.可选试剂:①Ca(OH)2溶液;②NaOH溶液;③饱和Na2CO3溶液;④肥皂水.实验方案:(填写下表)
(3)利用海水得到淡水的方法有蒸馏法、电渗析法等.电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示.
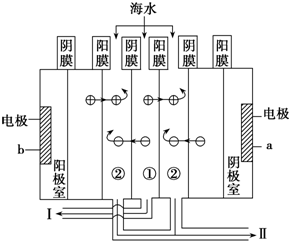
a接电源的负极,Ⅰ口排出的是淡水(填“淡水”或“海水”);
(4)在(3)中某口排出的浓海水中溴元素的质量分数为a%,现用氯气将其中的溴离子氧化为溴单质,则处理1 000t该浓海水需标准状况下的氯气的体积为1400am3.
(2)现有一杯具有永久硬度的水,其中主要含有MgCl2、CaCl2.利用下列试剂中的一部分或全部,设计软化该水的实验方案.可选试剂:①Ca(OH)2溶液;②NaOH溶液;③饱和Na2CO3溶液;④肥皂水.实验方案:(填写下表)
| 实验步骤 |
| 向硬水中加入①(填序数),直到不再产生沉淀为止. |
| 继续向溶液中加入③(填序数),直到不再产生沉淀为止. |
| 将上述混合物过滤(填操作) |

a接电源的负极,Ⅰ口排出的是淡水(填“淡水”或“海水”);
(4)在(3)中某口排出的浓海水中溴元素的质量分数为a%,现用氯气将其中的溴离子氧化为溴单质,则处理1 000t该浓海水需标准状况下的氯气的体积为1400am3.
11. 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1.
(2)分离高炉煤气得到的CO与空气可设计成燃料电池,若电解质为碱性.写出该燃料电池的负极反应式CO+4OH--2e-=CO32-+2H2O.
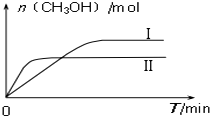
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);测得CH3OH的物质的量随时间的变化图:
①由图判断该反应△H< 0,曲线 I、II对应的平衡常数KI>KII(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为0.4<n(c)≤1.
③一定温度下,此反应在恒容密闭容器中进行,能判断该反应达到化学平衡状态的依据是a b.
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH)
d.容器中密度不变 e.2个C=O断裂的同时有3个C-H形成
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g).二甲醚可用作直接燃料电池,1mol二甲醚分子经过电化学氧化,可以产生12NA个电子的电量;根据化学反应原理,分析增加压强对制备二甲醚反应的影响该反应分子数减少,压强增加使平衡右移,CH3OCH3产率增加;压强增加使CO和H2浓度增加,反应速率增大.
 研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义.(1)CO可用于炼铁,已知:
Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1.
(2)分离高炉煤气得到的CO与空气可设计成燃料电池,若电解质为碱性.写出该燃料电池的负极反应式CO+4OH--2e-=CO32-+2H2O.
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);测得CH3OH的物质的量随时间的变化图:
①由图判断该反应△H< 0,曲线 I、II对应的平衡常数KI>KII(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡.
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
③一定温度下,此反应在恒容密闭容器中进行,能判断该反应达到化学平衡状态的依据是a b.
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH)
d.容器中密度不变 e.2个C=O断裂的同时有3个C-H形成
(4)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g).二甲醚可用作直接燃料电池,1mol二甲醚分子经过电化学氧化,可以产生12NA个电子的电量;根据化学反应原理,分析增加压强对制备二甲醚反应的影响该反应分子数减少,压强增加使平衡右移,CH3OCH3产率增加;压强增加使CO和H2浓度增加,反应速率增大.
9. 铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:
铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:
(1)该反应的平衡常数表达式K=$\frac{c(C{O}_{2})}{c(CO)}$;Q>0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.006mol/(L•min);
(3)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2. K2FeO4在处理水的过程中所起的作用有杀菌消毒、净水(吸附悬浮物);
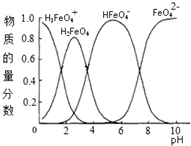
(4)高铁酸钾水溶液中FeO42-的存在形态及它们的物质的量分数随pH的变化如图所示:
(1)pH=2时溶液存在如下等量关系:c(K+)=2c(H2FeO4)+2c(H3FeO4+)+2c(HFeO4-);
(2)向pH=6的溶液中加入KOH溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42-+H2O.
 铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:
铁及其化合物在生产、生活中有广泛应用,如高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂;又知高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)+Q kJ,下表中是该反应在不同温度下的平衡常数:| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.006mol/(L•min);
(3)已知:4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2. K2FeO4在处理水的过程中所起的作用有杀菌消毒、净水(吸附悬浮物);
(4)高铁酸钾水溶液中FeO42-的存在形态及它们的物质的量分数随pH的变化如图所示:
(1)pH=2时溶液存在如下等量关系:c(K+)=2c(H2FeO4)+2c(H3FeO4+)+2c(HFeO4-);
(2)向pH=6的溶液中加入KOH溶液,发生反应的离子方程式为HFeO4-+OH-=FeO42-+H2O.
7.如图表示一定条件下反应N2(g)+3H2(g)?2NH3(g)△H<0的反应速率与反应过程的曲线关系图.下列说法正确的是( )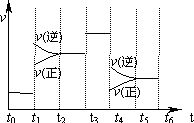

| A. | t2~t3和t3~t4时间段氨气的体积分数相等 | |
| B. | 氨气的体积分数最高的一段时间为t5~t6 | |
| C. | t4时刻改变的条件是降低温度 | |
| D. | t4~t5时间段平衡向正反应方向移动 |
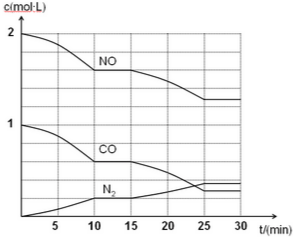
6.航天领域中常用N2H4与N2O4作为火箭发射的燃料与助燃剂.N2O4是一种无色气体,易分解:N2O4(g)?2NO2(g)-Q.N2H4与氨气相似,是一种碱性气体,易溶于水,生成弱碱N2H4•H2O.t℃时,将一定量的NO2、N2O4充入一个容积为2L的恒容密闭容器中,浓度随时间变化关系如下表所示:
(1)前10min内用NO2表示的反应速率为0.04mol•L-1•min-1;该反应的平衡常数表达式K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$.
(2)20min时改变的条件是向容器中加入0.8molNO2;重新达到平衡时,NO2的体积分数B(填字母)
A.增大B.减小C.不变D.无法判断
(3)用电离方程式表示N2H4•H2O显碱性的原因N2H4•H2O?N2H5++OH-(或N2H4+H2O?N2H5++OH-).
(4)相同条件下,1mol N2H4最多能与2mol HCl发生反应.
(5)常温下,若将0.2mol/LN2H4•H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H${\;}_{5}^{+}$、Cl-、OH-、H+四种离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
(提示:相同条件下,N2H4•H2O的电离程度大于N2H5Cl的水解程度.)
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/mol/L | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/mol/L | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
(2)20min时改变的条件是向容器中加入0.8molNO2;重新达到平衡时,NO2的体积分数B(填字母)
A.增大B.减小C.不变D.无法判断
(3)用电离方程式表示N2H4•H2O显碱性的原因N2H4•H2O?N2H5++OH-(或N2H4+H2O?N2H5++OH-).
(4)相同条件下,1mol N2H4最多能与2mol HCl发生反应.
(5)常温下,若将0.2mol/LN2H4•H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H${\;}_{5}^{+}$、Cl-、OH-、H+四种离子浓度由大到小的顺序为c(N2H5+)>c(Cl-)>c(OH-)>c(H+).
(提示:相同条件下,N2H4•H2O的电离程度大于N2H5Cl的水解程度.)
5.阿司匹林铜[Cu(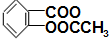 )2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(
)2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(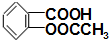 ,M=180)和Cu2+;
,M=180)和Cu2+;
已知:
实验一:阿司匹林铜的制备
阿司匹林$→_{②Naoh溶液}^{①95%乙醇}$阿司匹林钠$→_{15-20℃}^{CuSO_{4}溶液}$ $\stackrel{操作A}{→}$阿司匹林铜
实验二:阿司匹林铜纯度的测定
称取80℃干燥至恒重的阿司匹林铜样品1.0g,置于碘量瓶中,加5mL 6mol•L-1HCl,充分反应后加蒸馏水30mL摇匀,再加入2gKI摇匀,用0.1mol•L-1Na2S2O3溶液滴定至近终点时,加入100g•L-1KSCN试剂1mL,并加入2mL0.5%淀粉溶液,滴定至终点时共消耗Na2S2O3溶液体积为18.60mL.
已知:2Cu2++4I-═2CuI+I2;
I2+2S2O32-═2I-+S4O62-;
CuI+SCN-═CuSCN+I-
回答下列问题:
(1)Na2S2O3溶液应装在碱式滴定管中(填“酸式”或“碱式”);
(2)操作A包括三个实验操作,依次为过滤、洗涤、干燥;
(3)在实验一中采用不同原料比进行实验,得到下表的数据;
由此,实验时原料用量应控制阿司匹林过量;
(4)下列试剂中,洗涤阿司匹林铜最适宜的为B(填字母);
A.碳酸氢钠溶液 B.氯化铁溶液 C.红色石蕊试液 D.新制氢氧化铜悬浊液
(5)实验二中判断到达滴定终点的现象是滴入最后一滴Na2S2O3溶液,蓝色褪去,且半分钟内不恢复蓝色;
(6)碘化亚铜会强力吸附碘单质,实验中如果不加入KSCN试剂会使实验结果偏低(填“偏高”、“偏低”或“无影响”);
(7)阿司匹林铜样品的纯度为78.5%(保留小数点后面1位)
0 158935 158943 158949 158953 158959 158961 158965 158971 158973 158979 158985 158989 158991 158995 159001 159003 159009 159013 159015 159019 159021 159025 159027 159029 159030 159031 159033 159034 159035 159037 159039 159043 159045 159049 159051 159055 159061 159063 159069 159073 159075 159079 159085 159091 159093 159099 159103 159105 159111 159115 159121 159129 203614
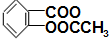 )2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(
)2]的消炎作用比阿司匹林强十多倍,它为亮蓝色结晶粉末,遇强酸解离为阿司匹林(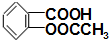 ,M=180)和Cu2+;
,M=180)和Cu2+;已知:
| 阿司匹林溶解质量 | 阿司匹林铜的溶解质量 | |
| 氯仿 | 0.4g | 不溶 |
| 无水乙醇 | 0.9g | 不溶 |
| 蒸馏水 | 不溶 | 不溶 |
阿司匹林$→_{②Naoh溶液}^{①95%乙醇}$阿司匹林钠$→_{15-20℃}^{CuSO_{4}溶液}$ $\stackrel{操作A}{→}$阿司匹林铜
实验二:阿司匹林铜纯度的测定
称取80℃干燥至恒重的阿司匹林铜样品1.0g,置于碘量瓶中,加5mL 6mol•L-1HCl,充分反应后加蒸馏水30mL摇匀,再加入2gKI摇匀,用0.1mol•L-1Na2S2O3溶液滴定至近终点时,加入100g•L-1KSCN试剂1mL,并加入2mL0.5%淀粉溶液,滴定至终点时共消耗Na2S2O3溶液体积为18.60mL.
已知:2Cu2++4I-═2CuI+I2;
I2+2S2O32-═2I-+S4O62-;
CuI+SCN-═CuSCN+I-
回答下列问题:
(1)Na2S2O3溶液应装在碱式滴定管中(填“酸式”或“碱式”);
(2)操作A包括三个实验操作,依次为过滤、洗涤、干燥;
(3)在实验一中采用不同原料比进行实验,得到下表的数据;
| 实验编号 | 阿司匹林:无水硫酸铜/物质的量之比 | 产率% | ||
| X1 | X2 | 平均值 | ||
| 1 | 1:1 | 76.6 | 78.1 | 77.4 |
| 2 | 2:1 | 78.6 | 75.1 | 76.8 |
| 3 | 3:1 | 93.9 | 95.9 | 94.9 |
(4)下列试剂中,洗涤阿司匹林铜最适宜的为B(填字母);
A.碳酸氢钠溶液 B.氯化铁溶液 C.红色石蕊试液 D.新制氢氧化铜悬浊液
(5)实验二中判断到达滴定终点的现象是滴入最后一滴Na2S2O3溶液,蓝色褪去,且半分钟内不恢复蓝色;
(6)碘化亚铜会强力吸附碘单质,实验中如果不加入KSCN试剂会使实验结果偏低(填“偏高”、“偏低”或“无影响”);
(7)阿司匹林铜样品的纯度为78.5%(保留小数点后面1位)
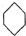 (g)?3H2(g)+
(g)?3H2(g)+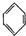 (g)△H1
(g)△H1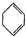 (g)△H2=+28.6KJ/mol
(g)△H2=+28.6KJ/mol