17.已知二甲苯的同分异构体有三种,从而可推知四氯苯的同分异构体数目是( )
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
13.下列转化不能一步实现的是( )
| A. | CuO→Cu(OH)2 | B. | Cu→CuSO4 | C. | MgSO4→MgCl2 | D. | NaCl→NaOH |
12.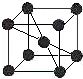 A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:
A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:
(1)E原子的基态电子排布式1s22s22p63s23p63d104s1或[Ar]3d104s1;
(2)A、B、C三种元素的第I电离能由大到小的顺序是N>O>Na,
(3)D能形成多种价态的含氧酸,其酸性由强到弱的顺序为HClO4>HClO3>HClO2>HClO.
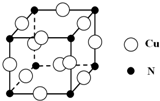
(4)已知金属C单质的晶胞为,则C原子的堆积方式为体心立方堆积,C原子的配位数是8,
(5)向E、D形成的稳定化合物溶液中不断加入A的常见氢化物水溶液,最后E的最主要存在形式为(写真实符号)Cu(NH3)42+.
 A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:
A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素.A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能.E是第四期第IB族元素,回答下列问题:| A | B | |
| D |
(2)A、B、C三种元素的第I电离能由大到小的顺序是N>O>Na,
(3)D能形成多种价态的含氧酸,其酸性由强到弱的顺序为HClO4>HClO3>HClO2>HClO.
(4)已知金属C单质的晶胞为,则C原子的堆积方式为体心立方堆积,C原子的配位数是8,
(5)向E、D形成的稳定化合物溶液中不断加入A的常见氢化物水溶液,最后E的最主要存在形式为(写真实符号)Cu(NH3)42+.
11.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )


| A. | 相对于途径②,途径①更好地体现了绿色化学思想 | |
| B. | X可能是SO2和SO3的混合气体 | |
| C. | Y可以是葡萄糖溶液 | |
| D. | 将CuSO4溶液蒸发,利用余热蒸干,可制得胆矾晶体 |
10.下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~(4)小题用元素符号或化学式回答,(5)~(8)小题按题目要求回答.
(1)表中元素,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是Na.
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是H2SO4,呈两性的是Al(OH)3.
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HCl.
(4)A和D组成化合物的电子式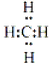 .
.
(5)用电子式表示B和H组成化合物的形成过程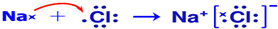
(6)B的最高价氧化物的水化物和C的最高价氧化物的水化物相互反应的离子方程式OH-+Al(OH)3═AlO2-+2H2O.
0 158891 158899 158905 158909 158915 158917 158921 158927 158929 158935 158941 158945 158947 158951 158957 158959 158965 158969 158971 158975 158977 158981 158983 158985 158986 158987 158989 158990 158991 158993 158995 158999 159001 159005 159007 159011 159017 159019 159025 159029 159031 159035 159041 159047 159049 159055 159059 159061 159067 159071 159077 159085 203614
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是H2SO4,呈两性的是Al(OH)3.
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HCl.
(4)A和D组成化合物的电子式
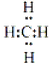 .
.(5)用电子式表示B和H组成化合物的形成过程
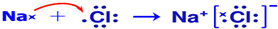
(6)B的最高价氧化物的水化物和C的最高价氧化物的水化物相互反应的离子方程式OH-+Al(OH)3═AlO2-+2H2O.
 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: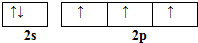 .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.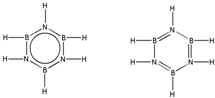 .
.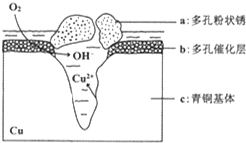 铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题: