9.下列各种醇不能被氧化成醛或酮的是(提示:酮的结构为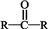 )( )
)( )
 )( )
)( )| A. | CH3OH | B. | 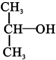 | C. | 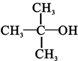 | D. | 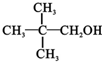 |
8.只用一种试剂即可鉴别C2H5OH、C6H5OH、AgNO3、Na2CO3、KI五种无色透明溶液,这种试剂是( )
| A. | 稀盐酸 | B. | 稀NaOH溶液 | ||
| C. | FeCl3溶液 | D. | 酸性高锰酸钾溶液 |
7.过量的锌粉与一定量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )
| A. | 加入适量的水 | B. | 适当升高温度 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入等体积的浓度较大的盐酸 |
6.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A. | 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 | |
| B. | 元素Y能与元素Z形成化合物Z2Y2,该化合物内部有两种化学键 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR,沸点XmY<XmR | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
4. 氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.
氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.
(1)获得硫酸铜:该小组同学利用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,从而获得硫酸铜,写出该反应的离子方程式:Cu+2H++H2O2═Cu2++2H2O.
(2)制备氧化铜:
粗CuSO4溶液(含有硫酸铁杂质)$\stackrel{步骤Ⅰ}{→}$纯CuSO4溶液$\stackrel{步骤Ⅱ}{→}$CuSO4•5H2O→…→CuO
已知:pH≥6.4时Cu(OH)2沉淀完全,而在pH=3~4时Fe(OH)3即能完全沉淀.
①步骤Ⅰ的目的是除去硫酸铁,可慢慢加入下列某些物质,搅拌,以控制溶液pH=3.5.加热煮沸一段时间,过滤,用稀硫酸酸化滤液至PH=1.下列物质有利于控制溶液PH=3.5的是AC.
A.Cu2(OH)2CO3粉末 B.Fe2O3粉末
C.Cu(OH)2固体 D.NaOH固体
②步骤Ⅱ的目的是得到CuSO4•5H2O固体,操作是蒸发浓缩、冷却结晶、过滤、水浴加热烘干.水浴加热的特点是受热更均匀,温度不会超过100℃.
(3)探究氧化铜的性质
探究氧化铜是否能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,实验时均以收集25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见表:
①上述实验中的“待测数据”指产生25mL气体所需时间.
②如何检查该装置的气密性:上下移动量气管,使量气管液出现高度差,一段时间后量气管中的液面差不变,则装置不漏气.
③为探究CuO在实验Ⅱ中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测CuO反应前后质量是否改变,b.CuO的化学性质有没有改变.
 氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.
氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.(1)获得硫酸铜:该小组同学利用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,从而获得硫酸铜,写出该反应的离子方程式:Cu+2H++H2O2═Cu2++2H2O.
(2)制备氧化铜:
粗CuSO4溶液(含有硫酸铁杂质)$\stackrel{步骤Ⅰ}{→}$纯CuSO4溶液$\stackrel{步骤Ⅱ}{→}$CuSO4•5H2O→…→CuO
已知:pH≥6.4时Cu(OH)2沉淀完全,而在pH=3~4时Fe(OH)3即能完全沉淀.
①步骤Ⅰ的目的是除去硫酸铁,可慢慢加入下列某些物质,搅拌,以控制溶液pH=3.5.加热煮沸一段时间,过滤,用稀硫酸酸化滤液至PH=1.下列物质有利于控制溶液PH=3.5的是AC.
A.Cu2(OH)2CO3粉末 B.Fe2O3粉末
C.Cu(OH)2固体 D.NaOH固体
②步骤Ⅱ的目的是得到CuSO4•5H2O固体,操作是蒸发浓缩、冷却结晶、过滤、水浴加热烘干.水浴加热的特点是受热更均匀,温度不会超过100℃.
(3)探究氧化铜的性质
探究氧化铜是否能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,实验时均以收集25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见表:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| KClO3质量 | 1.2g | 1.2g | 1.2g |
| 其他物质质量 | 无其他物质 | CuO 0.5g | MnO2 0.5g |
| 待测数据 |
②如何检查该装置的气密性:上下移动量气管,使量气管液出现高度差,一段时间后量气管中的液面差不变,则装置不漏气.
③为探究CuO在实验Ⅱ中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测CuO反应前后质量是否改变,b.CuO的化学性质有没有改变.
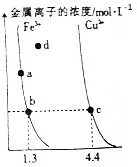
1.某温度下,Fe(OH)2和Cu(OH)2沉淀溶解平衡曲线如图所示,下列有关说法正确的是( )
0 158884 158892 158898 158902 158908 158910 158914 158920 158922 158928 158934 158938 158940 158944 158950 158952 158958 158962 158964 158968 158970 158974 158976 158978 158979 158980 158982 158983 158984 158986 158988 158992 158994 158998 159000 159004 159010 159012 159018 159022 159024 159028 159034 159040 159042 159048 159052 159054 159060 159064 159070 159078 203614

| A. | Ksp[Fe(OH)3]<Ksp[Cu(OH)2] | |
| B. | a、b、c、d四点的Kw不同 | |
| C. | 在Fe(OH)3饱和溶液中加入适量硝酸钾晶体可使a点变到b点 | |
| D. | d点时的Cu(OH)2溶液为不饱和溶液 |
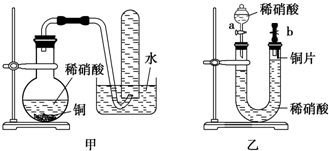
 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题: