3.下列有关化学反应类型的判断,错误的是( )
| 选项 | 化学方程式 | 反应类型 |
| A | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | 化合反应 |
| B | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | 分解反应 |
| C | BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2 | 复分解反应 |
| D | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | 置换反应 |
| A. | A | B. | B | C. | C | D. | D |
2.下列各组物质中,都属于混合物的是( )
| A. | 石灰水、水 | B. | 干冰、冰水混合物 | ||
| C. | 石墨、铁矿石 | D. | 不锈钢菜刀、食用醋 |
1.化学改变世界的途径是使物质发生化学变化.下列变化都属于化学变化的一组是( )
| A. | 酒精挥发酒精燃烧 | B. | 海水“制碱”海水“晒盐” | ||
| C. | 钢铁生锈冶炼钢铁 | D. | 葡萄酿酒葡萄榨汁 |
20.阿伏加德罗常数是物理学和化学中的一个重要常量.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,25.5g NH3所含的原子数为6NA | |
| C. | 标准状况下,11.2L水所含的分子数为0.5NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
19.工业上用软锰矿(主要成分为MnO2)和闪锌矿(主要成分为ZnS)制取干电池中所需的MnO2和Zn的工艺流程如下:
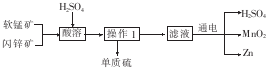
操作1过程中必须使用的仪器是( )

操作1过程中必须使用的仪器是( )
| A. | 蒸发皿 | B. | 漏斗 | C. | 蒸馏烧瓶 | D. | 容量瓶 |
18.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1molFe溶于硝酸,电子转移数为3NA | |
| B. | 12.0gNaHSO4固体中含阳离子数为0.1NA | |
| C. | 标准状态下,22.4L氟化氢中含有氟原子数为NA | |
| D. | 7.8gNa2O2与足量的水反应转移电子数为0.2NA |
17.下列说法正确的是( )
| A. | 1mol任何气体的体积都是22.4L | |
| B. | 1mol任何物质在标准状况下所占体积都约是22.4L | |
| C. | 1mol氯气、水、碘(I2)在标准状况下所含分子数相同 | |
| D. | 在同温同压下,相同质量的氯气和氢气的体积相同 |
15.元素A、B、C、D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;①x$\stackrel{z}{→}$p$\stackrel{w}{→}$q+z,②y$\stackrel{z}{→}$p+O2↑,其中z为液体、w为气体,其余均为固体.下列有关说法正确的是( )
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | y、p 中均只含有离子键 | |
| C. | B、D两元素最高价氧化物对应水化物分别为强酸、强碱 | |
| D. | p能抑制水的电离而q能促进水的电离 |
14.有关如图所示的两套电化学装置的说法正确的是( )

0 158878 158886 158892 158896 158902 158904 158908 158914 158916 158922 158928 158932 158934 158938 158944 158946 158952 158956 158958 158962 158964 158968 158970 158972 158973 158974 158976 158977 158978 158980 158982 158986 158988 158992 158994 158998 159004 159006 159012 159016 159018 159022 159028 159034 159036 159042 159046 159048 159054 159058 159064 159072 203614

| A. | 甲是原电池、乙是电解池 | |
| B. | 铜电极上的电极反应式均为Cu2++2e-=Cu | |
| C. | 甲装置放电效率高于乙装置 | |
| D. | 当有6.5 g Zn溶解时,乙装置中会有0.2 mol电子通过盐桥 |
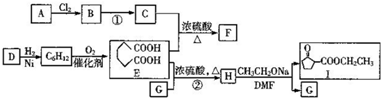
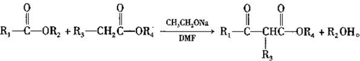
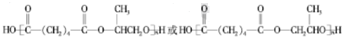 ,1中官能团的名称酯基和羰基.
,1中官能团的名称酯基和羰基.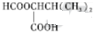 .
.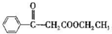 写出合成路线图.
写出合成路线图.