13.下列关于晶体结构的描述正确的是( )
| A. | 冰中存在极性键、非极性键、范德华力、氢键 | |
| B. | MCO3型碳酸盐,其分解温度越高,则分解后生成的金属氧化物的晶格能越大 | |
| C. | 等质量的金刚石晶体和石墨晶体含有的碳碳σ键数目相同 | |
| D. | 干冰的晶胞中CO2分子数目和金属铜的晶胞中Cu原子数目相同 |
12.下列关于化学式为[TiCl(H2O)5]Cl2•H2O的配合物的说法中正确的是( )
| A. | 配体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti3+,配离子是[TiCl(H2O)5]2+ | |
| C. | 内界和外界中的Cl-的数目比是 2:1 | |
| D. | 加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
11.下列说法中正确的是( )
| A. | 金刚石、碳化硅、晶体硅的熔点依次升高 | |
| B. | CO2和SiO2 化学式相似,物理性质也相似 | |
| C. | CH3CH(CH2OH)CH2OOCCH3是一种手性分子,水解后手性消失 | |
| D. | 水加热到很高的温度都难以分解是因为水分子间存在氢键 |
10.下列关于有机物的同分异构体的说法中,不正确的是(不考虑立体异构)( )
| A. | 分子式为C3H6Cl2的同分异构体有3种 | |
| B. | 分子式为C5H12O,且能与金属钠反应的同分异构体有8种 | |
| C. | 分子式为C4H8O2属于羧酸类的同分异构体有2种 | |
| D. | 分子式为C4H8O2属于酯类的同分异构体有4种 |
9.下列说法中正确的是(NA为阿伏加德罗常数的值)( )
| A. | 1mol苯分子中所含的C=C键数为3NA | |
| B. | 60gSiO2中含有Si-O键的个数为2NA | |
| C. | 0.1molCnH2n+2中含有的碳碳单键数为0.1nNA | |
| D. | 18 g冰中含氢键的个数为2NA |
8.下列有关化学用语的表示方法正确的有( )
①NaH电子式Na+[:H]-
②乙烯的结构式:CH2=CH2
③水分子的球棍模型:
④硫原子的外围电子排布式为3s23p4
⑤氟化铵的分子式:NH4F.
①NaH电子式Na+[:H]-
②乙烯的结构式:CH2=CH2
③水分子的球棍模型:

④硫原子的外围电子排布式为3s23p4
⑤氟化铵的分子式:NH4F.
| A. | ①③④ | B. | ①④ | C. | ②③⑤ | D. | 除② |
5.苹果酸的结构简式如图所示,下列说法正确的是( )
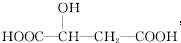
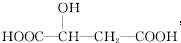
| A. | 苹果酸中能发生酯化反应的官能团有1种 | |
| B. | 1 mol苹果酸可与3 mol NaHCO3发生中和反应 | |
| C. | 1 mol苹果酸与足量金属 Na反应生成生成mol H2 | |
| D. | 1 mol苹果酸可以形成三元或四元环状内酯 |
4.下列说法正确的是( )(NA表示阿伏加德罗常数的值)
0 158871 158879 158885 158889 158895 158897 158901 158907 158909 158915 158921 158925 158927 158931 158937 158939 158945 158949 158951 158955 158957 158961 158963 158965 158966 158967 158969 158970 158971 158973 158975 158979 158981 158985 158987 158991 158997 158999 159005 159009 159011 159015 159021 159027 159029 159035 159039 159041 159047 159051 159057 159065 203614
| A. | 1mol石炭酸根含有的电子数目为49NA | |
| B. | 标况下1L已烷完全燃烧后恢复至原状态,生成气态物质分子数为6 NA22.4 | |
| C. | 1mol甲基含有9NA个电子 | |
| D. | 0.1mol甘油与足量的钠反应,可生成氢气3.36L |

 .
. .
.
 ;
; ;
; ;
; ;
; ;
; ;
;